题目内容
20.室温下,CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(1)△H1>0;CuSO4(s)=Cu2+(aq)+SO${\;}_{4}^{2-}$(aq)△H2<0.
若CuSO4•5H20受热分解的化学方程式为:CuSO4•5H2O(s)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4(s)+5H2O(l),热效应为△H3.则下列判断正确的是( )
| A. | △H1<△H3 | B. | △H2>△H3 | C. | △H1+△H3=△H2 | D. | △H1+△H2=△H3 |
分析 已知CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H1>0,CuSO4(s)=Cu2+(aq)+SO42-(aq)△H2<0,
CuSO4•5H2O(s)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4(s)+5H2O(l)△H3,根据盖斯定律确定关系.
解答 解:已知CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H1>0 ①,
CuSO4(s)=Cu2+(aq)+SO42-(aq)△H2<0 ②,
根据盖斯定律①-②得到CuSO4•5H2O(s)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4(s)+5H2O(l)△H3=△H1-△H2,因为△H1>0,△H2<0 故△H1<△H3,△H2<△H3,故A正确;
故选A.
点评 本题考查了化学反应的焓变以及盖斯定律的运用,题目较简单.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
10.化学与生活息息相关,下列说法正确的是( )
| A. | 我国居民传统膳食以糖类为主,淀粉、脂肪都是糖类物质 | |
| B. | 人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外 | |
| C. | 长期烧水的水壶内壁容易形成一层水垢,可以用食醋除去 | |
| D. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 |
15.足量的铁粉和热的稀HNO3反应,反应后溶液中只有Fe(NO3)2,并放出N2O气体2.24L(标准状况下),则反应中被氧化的铁粉质量是( )
| A. | 11.2g | B. | 22.4g | C. | 5.6g | D. | 56g |
5.常温下,下列说法正确的是( )
| A. | 向Na2CO3溶液中加入等浓度等体积的盐酸:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | NaHS溶液中:c(OH-)+c(S2-)=c(H+)+c(H2S) | |
| C. | pH相同的①CH3COONa溶液、②NaClO溶液中c(Na+):①<② | |
| D. | pH=9的0.1mol•L-1的NaHR溶液中:c(HR-)>c(H+)>c(R2-)>c(H2R) |
1.某探究小组用测量HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.限选试剂:1.00mol•L-1HNO、2.00mol•L-1HNO3、细颗粒大理石、粗颗粒大理石\35℃水浴.
(1)依据题给条件.你认为他们能完成哪些因素对速率形响的探究?HNO3浓度、温度、大理石的表面积.
(2)请根据(I)中选择的探究内容.填写以下实验设计表.完成探究实验:
 (3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.
(3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.
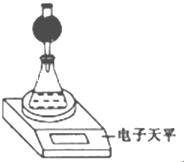
(4)该实验小组用如图实验装置进行实验.
①除电于天平、干燥管、锥形瓶、药匙、胶塞等仪器外.必需的实验仪器还有量筒、秒表.干燥管中放置的试剂可以是bc(填序号).
a.碱石灰 b.无水CaCl2 c.P2O5固体 d.浓硫酸
③若撤除干燥管装置,所测速率偏大(填“偏大”“偏小”或“不变”).
(1)依据题给条件.你认为他们能完成哪些因素对速率形响的探究?HNO3浓度、温度、大理石的表面积.
(2)请根据(I)中选择的探究内容.填写以下实验设计表.完成探究实验:
| 实验编号 | T/℃ | 大理石规格 | HNO3浓度/mol•L-1 |
| ① | 常温 | 2.00 | |
| ② | 1.00 | ||
| ③ | 2.00 | ||
| ④ | 2.00 |
 (3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.
(3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.(4)该实验小组用如图实验装置进行实验.
①除电于天平、干燥管、锥形瓶、药匙、胶塞等仪器外.必需的实验仪器还有量筒、秒表.干燥管中放置的试剂可以是bc(填序号).
a.碱石灰 b.无水CaCl2 c.P2O5固体 d.浓硫酸
③若撤除干燥管装置,所测速率偏大(填“偏大”“偏小”或“不变”).

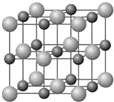 原子序数小于36的X、Y、Z和铜四种元素,X的基态原子有3个不同的能级,有一个能级中的电子数比其它两个能级的中电子数都多1;Y基态原子中的电子占有5个轨道,其中有2个轨道处于半满状态,Z的原子序数为24.
原子序数小于36的X、Y、Z和铜四种元素,X的基态原子有3个不同的能级,有一个能级中的电子数比其它两个能级的中电子数都多1;Y基态原子中的电子占有5个轨道,其中有2个轨道处于半满状态,Z的原子序数为24. .
.