题目内容
下列说法中正确的是( )
| A、标准状况下,1mol水的体积是22.4 L |
| B、1mol任何气体,体积均为22.4L |
| C、在标准状况下,0.3mol N2和0.7mol O2混合气体总体积约为22.4L |
| D、通常状况下,1mol N2的体积约为22.4L |
考点:气体摩尔体积
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标准状况水不是气体
B、温度压强不知气体摩尔体积不一定是22.4L/mol;
C、0.3mol N2和0.7mol O2混合气体为1mol,依据标准状况气体摩尔体积计算气体体积;
D、标准状况下,1mol N2的体积约为22.4L.
B、温度压强不知气体摩尔体积不一定是22.4L/mol;
C、0.3mol N2和0.7mol O2混合气体为1mol,依据标准状况气体摩尔体积计算气体体积;
D、标准状况下,1mol N2的体积约为22.4L.
解答:
解:A、标准状况水不是气体,1mol水的体积不是22.4 L,故A错误;
B、温度压强不知,气体摩尔体积不一定是22.4L/mol,标准状况1mol水的体积是22.4 L,故B错误;
C、0.3mol N2和0.7mol O2混合气体为1mol,依据标准状况气体摩尔体积计算气体在标准状况下,0.3mol N2和0.7mol O2混合气体总体积约为22.4L,故C正确;
D、标准状况下,1mol N2的体积约为22.4L,通常状况1mol N2的体积不是22.4L,故D错误;
故选C.
B、温度压强不知,气体摩尔体积不一定是22.4L/mol,标准状况1mol水的体积是22.4 L,故B错误;
C、0.3mol N2和0.7mol O2混合气体为1mol,依据标准状况气体摩尔体积计算气体在标准状况下,0.3mol N2和0.7mol O2混合气体总体积约为22.4L,故C正确;
D、标准状况下,1mol N2的体积约为22.4L,通常状况1mol N2的体积不是22.4L,故D错误;
故选C.
点评:本题考查了气体摩尔体积概念分析判断,条件分析应用,掌握概念实质是关键,题目较简单.

练习册系列答案
相关题目
下列实验所对应的离子方程式正确的是( )
| A、向NaAlO2溶液中通入少量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| B、向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O═Fe(OH)3↓+3H+ |
| C、在碳酸氢钡溶液中加入过量的氢氧化钠溶液:Ba2++2HCO3-+2OH-═BaCO3↓+CO32-+2H2O |
| D、向FeCl2溶液中加入少量K3[Fe(CN)6]溶液:4Fe2++2[Fe(CN)6]4-═Fe4[Fe(CN)6]2↓ |
某同学用50mL 0.50mol?L-1的盐酸与50mL0.55mol?L-1的氢氧化钠溶液进行中和反应并计算中和热.造成测得的结果偏高的原因可能是( )
| A、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 |
| B、做本实验的当天室温较高 |
| C、将50mL 0.55mol?L-1的氢氧化钠溶液取成了50mL 0.55mol?L-1的氨水 |
| D、在量取盐酸时仰视读数 |
下列说法正确的是( )
A、NaHCO3溶液加水稀释,
| ||
| B、1 mol?L-1的NH4Cl溶液中含有NH4+的数目一定小于NA | ||
| C、用石墨电极电解FeCl3溶液,阴极反应:2Fe3++6H2O+6e-═2Fe(OH)3↓+3H2↑ | ||
| D、将带有相反电荷的胶体混合,一定会出现胶体聚沉现象 |
在0.6mol Ba(OH)2中,含有OH-的数目是( )
| A、约为1.2 |
| B、约为7.22×1023 |
| C、约为6.02×1023 |
| D、约为3.01×1023 |
下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为( )
| A、纯盐酸、空气、硫酸、干冰 |
| B、蒸馏水、氨水、碳酸氢钠、二氧化硫 |
| C、胆矾、盐酸、铁、碳酸钙 |
| D、生石灰、漂白粉、氯化铜、碳酸钠 |
下列关于电解质溶液的说法正确的是( )
| A、将等物质的量浓度的NaHCO3与Na2CO3溶液等体积混合,所得混合液中有:c(CO32-)+2c(OH-)═2c(H+)+c(HCO3-)+3c(H2CO3) |
| B、1L pH=3的H2SO4溶液与10L Ba(OH)2溶液恰好完全反应,则Ba(OH)2溶液的pH一定等于10 |
| C、NaHS溶液呈碱性,是因HS-发生水解,其水解离子方程式为:HS-+H2O?S2-+H3O+ |
| D、pH=9的CH3COONa溶液和pH=9的NH3?H2O溶液,两溶液中水的电离程度相同 |
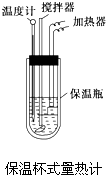 在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1. 已知A、B、C、D、E、F、G七种元素,它们的原子序数依次增大,A在所有元素中原子半径最小,B原子核外电子有6种不同运动状态;D与C、E均相邻;A、D、E三种元素的原子序数之和为25;E2-和F+有相同的核外电子排布;G的质子数是25.请回答下列问题:
已知A、B、C、D、E、F、G七种元素,它们的原子序数依次增大,A在所有元素中原子半径最小,B原子核外电子有6种不同运动状态;D与C、E均相邻;A、D、E三种元素的原子序数之和为25;E2-和F+有相同的核外电子排布;G的质子数是25.请回答下列问题: