题目内容
7.某同学将一小块钠放入盛有硫酸铜溶液的烧杯中,下列现象描述错误的是( )| A. | 钠浮在水面上,四处游动 | |
| B. | 反应放出的热量使得钠熔化成一个小球 | |
| C. | 反应完后烧杯中有蓝色不溶物 | |
| D. | 反应完后烧杯中出现红色不溶物 |
分析 Na的密度小于水,熔点较低,Na先与溶液中的H2O剧烈反应生成H2和NaOH,且同时放出大量热,NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,据此分析解答.
解答 解:Na的密度小于水,熔点较低,Na先与溶液中的H2O剧烈反应生成H2和NaOH,且同时放出大量热,放出的热量使钠熔成小球,钠受力不均导致其四处游动,生成的NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,
A.通过以上分析知,钠熔成小球并在液面上游动,故A不选;
B.钠和水反应生成氢气,所以有气体生成,放出热量,钠的溶点低,所以反应放出的热量使得钠熔化成一个小球,故B不选;
C.NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,溶液中铜离子浓度降低,所以溶液颜色变浅且有蓝色沉淀生成,故C不选;
D.NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,所以Na不会置换出Cu,故D选;
故选D.
点评 本题考查钠的性质,侧重考查元素化合物知识,明确反应先后顺序是解本题关键,注意在金属活动性顺序表中K、Ca、Na不能置换出其后面金属盐溶液中的金属单质,为易错点.

练习册系列答案
相关题目
17.下列离子方程式书写正确的是( )
| A. | CaCO3与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铁与硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| D. | 锌与硫酸铜溶液反应:Zn+Cu2+═Zn2++Cu |
18.下列属于温室气体的是( )
| A. | O2 | B. | CO | C. | N2 | D. | CO2 |
2.下列有关铁及其化合物的说法中正确的是( )
| A. | 赤铁矿的主要成分是Fe3O4 | |
| B. | 铁与水蒸气在高温下的反应产物为Fe2O3和H2 | |
| C. | Fe(OH)2不稳定,在潮湿的空气中很容易被氧化 | |
| D. | 含Fe2+的溶液滴加KSCN后溶液变红色 |
12.下表中列出了25℃、101kPa时一些物质的燃烧热数据
已知键能:C-H键:413.4kJ/mol、H-H键:436.0kJ/mol.则下列叙述正确的是( )
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/kJ/mol | 890.3 | 1299.6 | 285.8 |
| A. | CH4(g)+2O2(g)═CO2 (g)+2 H2O ( l)△H=-890.3 kJ/mol | |
| B. | 质量相等的CH4比C2H2燃烧放出热量少 | |
| C. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ/mol | |
| D. | 2CH4(g)═C2H2(g)+3H2(g)△H=-376.4 kJ/mol |
19.目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”.某研究性学习小组拟对融雪氯盐(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究.
该小组设计流程如图:
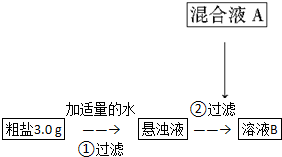
(1)加入混合液A的主要成分是NaOH、Na2CO3(填化学式).
(2)为检验溶液B中的Mg2+、Ca2+,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+,向其中一支试管中加入NaOH溶液(填化学式),看是否有沉淀生成.
步骤二:检验Ca2+,向另一支试管中加入某溶液,看是否有沉淀生成.下列三种溶液,其沉淀效果最好的是A.
A.0.1mol•L-1 Na2CO3溶液 B.0.1mol•L-1Na2SO3溶液 C.0.1mol•L-1 Na2C2O4溶液
(3)在除杂过程中,向粗盐悬浊液中加混合液A时需控制溶液pH=12以确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在1.8×10-7mol•L-1以下.
(4)对溶液B加热并不断滴加6mol•L-1的盐酸,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C.该操作的目的是除去NaOH和Na2CO3.
(5)溶液C倒入蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到有大量固体析出时停止加热.
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 6.8×10-8 | 4.0×10-9 | 1.8×10-11 |

(1)加入混合液A的主要成分是NaOH、Na2CO3(填化学式).
(2)为检验溶液B中的Mg2+、Ca2+,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+,向其中一支试管中加入NaOH溶液(填化学式),看是否有沉淀生成.
步骤二:检验Ca2+,向另一支试管中加入某溶液,看是否有沉淀生成.下列三种溶液,其沉淀效果最好的是A.
A.0.1mol•L-1 Na2CO3溶液 B.0.1mol•L-1Na2SO3溶液 C.0.1mol•L-1 Na2C2O4溶液
(3)在除杂过程中,向粗盐悬浊液中加混合液A时需控制溶液pH=12以确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在1.8×10-7mol•L-1以下.
(4)对溶液B加热并不断滴加6mol•L-1的盐酸,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C.该操作的目的是除去NaOH和Na2CO3.
(5)溶液C倒入蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到有大量固体析出时停止加热.
17.有机化学知识在生活中应用广泛,下列说法不正确的是( )
| A. | 纤维素可在人体内水解成葡萄糖 | |
| B. | 由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分 | |
| C. | 用灼烧的方法可以鉴别毛织物和棉织物 | |
| D. | 油脂是产生能量最高的营养物质,在饮食中不必控制油脂的摄入量 |

 .
. .
.