题目内容
3.粗盐提纯制精盐的实验中,不需要的操作是( )| A. | 溶解 | B. | 过滤 | C. | 洗涤 | D. | 蒸馏 |
分析 粗盐中含难溶的泥沙以及可溶性杂质(钙离子、镁离子、硫酸根),通过溶解、添加除掉可溶性杂质的试剂,将其沉淀下来,过滤,便可除掉难溶性杂质泥沙,还有可溶性杂质也转化成了难溶的沉淀,对沉淀进行洗涤,可以减小氯化钠的损失.所得滤液进行蒸发结晶,而不是蒸馏.
解答 解:A.粗盐中含难溶的泥沙以及可溶性杂质(钙离子、镁离子、硫酸根),通过溶解、添加除掉可溶性杂质的试剂:过量的氢氧化钠溶液、过量的氯化钡溶液、过量的碳酸钠溶液,将钙离子、镁离子、硫酸根离子沉淀下来,再过滤,便可除掉难溶性杂质泥沙,还有可溶性杂质也转化成了难溶的沉淀,故A正确.
B.根据A的分析一定需要过滤的,故B正确.
C.对沉淀可进行洗涤,减小氯化钠的损失,故C正确.
D.将所得滤液进行蒸发结晶,而不是蒸馏.蒸馏在整个实验中不需要,故D错误.
故选D.
点评 粗盐提纯(包括制精盐)实验中用到的操作有溶解、过滤、蒸发结晶,这是中学最精典的分离提纯实验操作,题目较简单.

练习册系列答案
相关题目
18.标准状况下,乙烷与炔烃X组成的混合烃22.4L与过量的氧气混合并完全燃烧,通过浓硫酸后,恢复到原来的温度,气体的总体积缩小了44.8L,则炔烃X是( )
| A. | C2H2 | B. | C3H4 | C. | C4H6 | D. | C5H8 |
15.在如图装置中,铁片上没有气泡产生的是( )
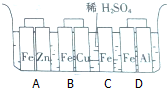

| A. | A | B. | B | C. | C | D. | D |
2.下列体系加压后,对化学反应速率没有影响的是( )
| A. | 2SO2+O2?2SO3 | B. | CO+H20(气)?CO2+H2 | ||
| C. | CO2+H2O?H2CO3 | D. | NaOH+HCl=NaCl+H20 |
15.下列化学用语表达正确的是( )
| A. | 溴化铵的电子式: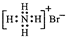 | B. | CO2的电子式: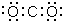 | ||
| C. | HClO的结构式:H-Cl-O | D. | 氮分子的结构式:N≡N |
12.有短周期元素X、Y、Z、D、E,其中X、Y、Z、D在周期表中的相对位置如下表,已知X与Y的原子序数之和等于Z的核电荷数,E与Z为同周期元素,0.2mol E与足量盐酸反应,得到2.24L气体(标准状况).回答下列问题:
(1)写出元素名称:X氮,E钠.
(2)X、D的氢化物相遇时产生的现象是冒白烟.
(3)X的最高价氧化物的水化物M,其稀溶液能与Z的低价氧化物反应,离子方程式为2NO3-+3SO2+2H2O═4H++2NO↑+3SO42-,则M的稀溶液的氧化性大于Z的最高价氧化物的水化物的稀溶液的氧化性(填“大于”、“等于”或“小于”).
(4)E的某种氧化物能与水发生氧化还原反应,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑.0.1mol E的该氧化物完全反应,转移电子数目为0.1NA.
| X | Y | |
| Z | D |
(2)X、D的氢化物相遇时产生的现象是冒白烟.
(3)X的最高价氧化物的水化物M,其稀溶液能与Z的低价氧化物反应,离子方程式为2NO3-+3SO2+2H2O═4H++2NO↑+3SO42-,则M的稀溶液的氧化性大于Z的最高价氧化物的水化物的稀溶液的氧化性(填“大于”、“等于”或“小于”).
(4)E的某种氧化物能与水发生氧化还原反应,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑.0.1mol E的该氧化物完全反应,转移电子数目为0.1NA.
13.常温下,对于pH均为9的NaOH溶液CH3COONa溶液,下列说法正确的是( )
| A. | 两溶液稀释10倍后,pH相等 | |
| B. | 两溶液加热至相同的温度后,pH相等 | |
| C. | 两溶液中各加入等体积的pH等于5的HCl溶液后,pH相等 | |
| D. | 两溶液中水的离子积相等 |
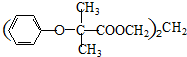
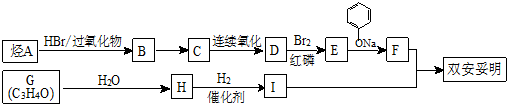
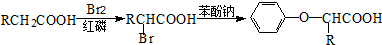
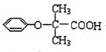 .
.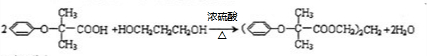 .
. .
.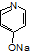 (
(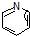 与
与 苯环性质相似)与
苯环性质相似)与 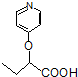 合成的路线:
合成的路线: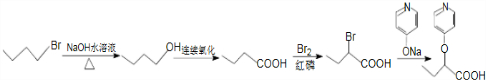 .
. 某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.