题目内容
1.铁钉与碳棒用导线连接后,同时浸入0.1mol•L-1的NaCl溶液中,可能发生的反应是( )| A. | 碳棒上放出氯气 | B. | 碳棒上放出氧气 | C. | 碳棒附近产生OH- | D. | 铁钉被还原 |
分析 铁钉与碳棒在氯化钠溶液中发生吸氧腐蚀,其中铁是负极,碳棒是正极,以此解答.
解答 解:铁和碳棒构成原电池,由于氯化钠溶液显中性,所以发生钢铁的吸氧腐蚀,其中铁是负极,电极反应为Fe-2e-=Fe2+,铁被氧化;
碳棒是正极,反应式为O2+4e-+2H2O=4OH-,由正极反应可知碳棒附近产生OH-,
故选C.
点评 本题考查金属的吸氧腐蚀,是基础性试题的考查,难度不大,主要是检验学生对基础知识的理解掌握程度,以及灵活运用知识的能力.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
11.下列关于钠及其化合物的叙述错误的是?( )
| A. | 取用金属钠时,所需用品至少有小刀、镊子、滤纸、玻璃片 | |
| B. | 金属钠与Ca(HCO3)2溶液反应时,既有白色沉淀又有气体逸出 | |
| C. | 生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl | |
| D. | Na2O2与碱反应生成盐和水,所以Na2O2是碱性氧化物 |
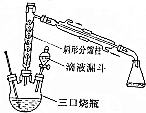
9.乙酸乙酯时重要的工业溶剂,也是生产醋酸纤维、合成药物的原料.实验室制备乙酸乙酯的反应装置示意图和有关数据如下:
实验步骤:
①在三颈烧瓶中,加入10mL乙醇,在振摇下分次加入10mL浓硫酸,混合均匀,加入几粒沸石,按图示装配好各仪器.
②在沙浴小心加热三颈烧瓶,反应温度约为110℃.
③将20mL冰醋酸与20mL乙醇的混合物由液滴漏斗滴入三颈烧瓶中.
④把收集到的溶液用20mL2mol•L-1碳酸钠溶液洗涤2~3次,再用水洗涤.
⑤分液,上面酯层倒入干燥的50mL锥形瓶中,加适量无水硫酸镁,加塞,放置,过滤,得乙酸乙酯粗品.回
答下列问题:
(1)装置中分馏柱的作用是冷凝回流;加入沸石的目的是防止爆沸.
(2)该实验为了提高乙酸的转化率和乙酸乙酯和产率,可采取的措施有使用浓硫酸吸水、把酯蒸出反应体系、提高醇的用量等(填字母).
 | 物质 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 水的溶解性 |
| 乙醇 | 46 | 0.789 | 78.3 | 溶 | |
| 乙酸 | 60 | 1.050 | 117.9 | 溶 | |
| 乙酸乙酯 | 88 | 0.896 | 77.2 | 不溶 |
①在三颈烧瓶中,加入10mL乙醇,在振摇下分次加入10mL浓硫酸,混合均匀,加入几粒沸石,按图示装配好各仪器.
②在沙浴小心加热三颈烧瓶,反应温度约为110℃.
③将20mL冰醋酸与20mL乙醇的混合物由液滴漏斗滴入三颈烧瓶中.
④把收集到的溶液用20mL2mol•L-1碳酸钠溶液洗涤2~3次,再用水洗涤.
⑤分液,上面酯层倒入干燥的50mL锥形瓶中,加适量无水硫酸镁,加塞,放置,过滤,得乙酸乙酯粗品.回
答下列问题:
(1)装置中分馏柱的作用是冷凝回流;加入沸石的目的是防止爆沸.
(2)该实验为了提高乙酸的转化率和乙酸乙酯和产率,可采取的措施有使用浓硫酸吸水、把酯蒸出反应体系、提高醇的用量等(填字母).
16.关于物质的量的叙述正确的是( )
| A. | 常温常压下,4.4g CO2物质的量为0.1mol | |
| B. | 常温常压下,6.2g Na2O含有的Na+离子数为0.1mol | |
| C. | 标准状况下,1NA个H2O分子含有氧分子数为1mol | |
| D. | 标准状况下,22.4L酒精的物质的量为1mol |
6.室温下,某碱溶液中水电离出的c(OH-)与某酸溶液中水电离出的c(OH-)相等,将两溶液等体积混合,混合溶液的pH是( )
| A. | 小于7 | B. | 等于7 | ||
| C. | 大于7 | D. | 可能等于7,也可能于小于7或大于7 |