题目内容
6.室温下,某碱溶液中水电离出的c(OH-)与某酸溶液中水电离出的c(OH-)相等,将两溶液等体积混合,混合溶液的pH是( )| A. | 小于7 | B. | 等于7 | ||
| C. | 大于7 | D. | 可能等于7,也可能于小于7或大于7 |
分析 室温下,某碱溶液中水电离出的c(OH-)与某酸溶液中水电离出的c(OH-)相等,说明碱溶液中的c(OH-)与酸溶液中的c(H+)相等,根据酸和碱的强弱性来讨论酸碱混合后的反应情况,据此分析.
解答 解:室温下,某碱溶液中水电离出的c(OH-)与某酸溶液中水电离出的c(OH-)相等,说明碱溶液中的c(OH-)与酸溶液中的c(H+)相等.
①若碱为强碱、酸为强酸,则碱溶液中的c(OH-)与酸溶液中的c(H+)均为两溶液中的全部氢氧根和氢离子,故两者等体积混合后恰好完全反应生成强酸强碱盐,溶液显中性,pH=7;
②若碱为弱碱、酸为强酸,则碱溶液中的c(OH-)是电离出的氢氧根,酸溶液中的c(H+)为溶液中的全部氢离子,故两者等体积混合后,碱过量,溶液显碱性,pH>7;
③若碱为强碱、酸为弱酸,则碱溶液中的c(OH-)为溶液中的全部氢氧根,酸溶液中的c(H+)是电离出的氢离子,故两者等体积混合后酸过量,溶液显酸性,pH<7;
④若碱为弱碱、酸也为弱酸,则根据碱和酸的相对强弱,所得溶液也可能为中性、酸性和碱性.
综上分析可知,溶液混合后pH可能等于7,也可能大于7或小于7,故选D.
点评 本题考查了酸和碱混合后溶液pH的计算,根据酸和碱的强弱来分类讨论,难度不大.

练习册系列答案
相关题目
16.甲、乙、丙、丁4种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、HCO3-、SO42-、OH-、Cl-中的不同阳离子和阴离子各一种组成.已知:①将足量的甲溶液分别与其他3种物质的溶液混合,均有白色沉淀生成;②0.1mol?L-1乙溶液中c(H+)>0.1mol?L-1;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成.下列结论正确的是( )
| A. | 甲溶液含有Ba2+ | B. | 乙溶液不含SO42- | C. | 丙溶液含有HCO3- | D. | 丁溶液含有Mg2+ |
17.已知溴(Br2)的性质与Cl2相似,将溴水加人含有下列离子的溶液中,离子浓度变化最小的是( )
| A. | Fe2+ | B. | HCO3- | C. | Fe3+ | D. | OH- |
14.下列有关物质性质的描述正确的是( )
| A. | 非金属氧化物都不能与酸反应 | B. | 含金属元素的盐溶液一定呈酸性 | ||
| C. | 组成元素相同的盐溶液酸碱性相同 | D. | 非金属元素可能形成离子化合物 |
1.铁钉与碳棒用导线连接后,同时浸入0.1mol•L-1的NaCl溶液中,可能发生的反应是( )
| A. | 碳棒上放出氯气 | B. | 碳棒上放出氧气 | C. | 碳棒附近产生OH- | D. | 铁钉被还原 |
11.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
(1)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5mol O2发生如下反应:4NO2(g)+O2(g)?2N2O5(g);已知体系中n(NO2)随时间变化如表:
①写出该反应的逆反应的平衡常数表达式:K=$\frac{c{\;}^{2}(N{\;}_{2}O{\;}_{5})}{{c}^{4}(NO{\;}_{2})•c(O{\;}_{2})}$.
已知:K300℃>K350℃,则该反应是放热反应(填“放热”或“吸热”);
②反应达到平衡后,NO2的转化率为49.6%,若要增大NO2的转化率,可采取的措施有BC.
A.再充入NO2 B.再充入4mol NO2和1mol O2
C.降低温度 D.充入氦气
③图1中表示N2O5的浓度的变化曲线是c;
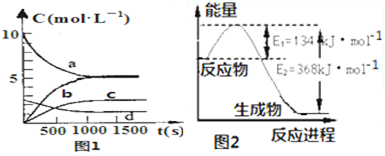
(2)图2是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图;又已知:
2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-760.3kJ•mol-1,
则反应:N2 (g)+2NO2 (g)?4NO(g) 的△H=+292.3kJ•mol-1.
(1)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5mol O2发生如下反应:4NO2(g)+O2(g)?2N2O5(g);已知体系中n(NO2)随时间变化如表:
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
已知:K300℃>K350℃,则该反应是放热反应(填“放热”或“吸热”);
②反应达到平衡后,NO2的转化率为49.6%,若要增大NO2的转化率,可采取的措施有BC.
A.再充入NO2 B.再充入4mol NO2和1mol O2
C.降低温度 D.充入氦气
③图1中表示N2O5的浓度的变化曲线是c;

(2)图2是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图;又已知:
2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-760.3kJ•mol-1,
则反应:N2 (g)+2NO2 (g)?4NO(g) 的△H=+292.3kJ•mol-1.
18.在无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+、Na+、ClO、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | Mg2+、NH4+、Cl-、SO42- |
15.常温下,有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的盐酸;③pH=11的氨水;④pH=11的NaOH溶液.下列说法正确的是( )
| A. | ④和②混合溶液中:c(H+)=c(OH-) | |
| B. | ①与④混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | ②和③混合溶液中:c(H+)>c(OH-) | |
| D. | 四种溶液稀释100倍,溶液pH:③>④>②>① |