题目内容
13.标准状况下,某气体的密度为1.964g/L,求该气体的摩尔质量.分析 一种物质的摩尔质量即单位物质的量的物质所具有的质量,据此分析.
解答 解:在标况下,1mol气体的体积为22.4L,故1mol此气体的质量m=ρV=1.964g/L×22.4L=44g,由于一种物质的摩尔质量即单位物质的量的物质所具有的质量,故此气体的摩尔质量为44g/mol.
答:此气体的摩尔质量为44g/mol.
点评 本题考查了物质摩尔质量的计算,应注意的是单位物质的量的物质所具有的质量即为此物质的摩尔质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.电渗析法是指在外加电场作用下,利用阴离子交换膜和阳离子交换膜的选择透过性,使部分离子透过离子交换膜而迁移到另一部分水中,从而使一部分水淡化而另一部分水浓缩的过程.下图是利用电渗析法从海水中获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为石墨电极.下列有关描述错误的是( )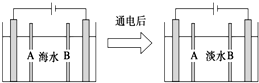

| A. | 阳离子交换膜是A,不是B | |
| B. | 通电后阳极区的电极反应式:2Cl--2e-═Cl2↑ | |
| C. | 工业上阴极使用铁丝网代替石墨碳棒,增大反应接触面 | |
| D. | 阴极区的现象是电极上产生无色气体,溶液中出现少量白色沉淀 |
4.将20mL0.8mol•L-1H2SO4溶液加水稀释到100mL,稀释后H2SO4溶液中的物质的量浓度为( )
| A. | 0.2mol•L-1 | B. | 0.16mol•L-1 | C. | 0.32mol•L-1 | D. | 0.08mol•L-1 |
1.铁钉与碳棒用导线连接后,同时浸入0.1mol•L-1的NaCl溶液中,可能发生的反应是( )
| A. | 碳棒上放出氯气 | B. | 碳棒上放出氧气 | C. | 碳棒附近产生OH- | D. | 铁钉被还原 |
8.莫尔盐[(NH4)2Fe(SO4)2•6H2O]常作氧化还原滴定法的基准物质,在0.1mol/L 的该盐的溶液中,下列有关比较正确的是( )
| A. | c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | B. | c(H+)=c(OH-)+c(NH3•H2O) | ||
| C. | c(SO42-)+c(OH-)=c(NH4+)+c(Fe2+)+c(H+) | D. | c(NH3•H2O)+c(NH4+)=0.1 mol/L |
18.在无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+、Na+、ClO、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | Mg2+、NH4+、Cl-、SO42- |
2.天然纤维的吸湿性优于合成纤维,合成纤维中吸湿性较好的是( )
| A. | 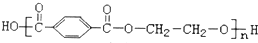 涤纶 涤纶 | B. | 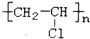 氯纶 氯纶 | ||
| C. | 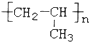 丙纶 丙纶 | D. | 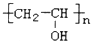 维纶 维纶 |