题目内容
13.下列物质的水溶液能导电,但属于非电解质的是( )| A. | CH3COOH | B. | Br2 | C. | SO2 | D. | NH4HCO3 |
分析 电解质是指在水溶液或熔化状态下能导电的化合物,而非电解质是指在水溶液和熔化状态下都不能导电的化合物,据此判断.
解答 解:A.乙酸属于电解质,故A不选;
B.Br2是单质,既不是电解质,也不是非电解质,故B不选;
C.SO2属于非电解质,溶于水,与水反应生成一水合氨,一水合氨电离产生自由离子而导电,故C选;
D.碳酸氢铵是电解质,故D不选;
故选:C.
点评 本题考查电解质和非电解质,学生应明确电解质和非电解质都是化合物,并明确判断电解质时发生电离的为化合物本身来分析解答即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列说法错误的是( )
| A. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| B. | 放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小 | |
| C. | 已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;则△H1>△H2 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
4.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的己烷所含的分子数为0.5NA | |
| B. | 28g乙烯在氧气中完全燃烧消耗氧气分子的数目为3NA | |
| C. | 1mol甲基(-CH3)所含的电子总数为10NA | |
| D. | 分子式为C2H6O中含有C-H(碳氢键)的数目为6NA |
8.下列说法正确的是( )
| A. | NaHSO3和NaHCO3的混合溶液中(S和C均用R表示):c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-) | |
| B. | 常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中水的电离程度:③>①>② | |
| C. |  常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
5.据某科学杂志报道,国外有一研究发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60的结构.下列叙述正确的是( )
| A. | 该物质有很高的熔点、很大的硬度 | |
| B. | 该物质形成的晶体属分子晶体 | |
| C. | 该物质分子中Si60被包裹在C60里面 | |
| D. | C60易溶于水 |
2.下列物质属于芳香烃,但不是苯的同系物的是( )
①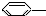 CH3 ②
CH3 ②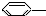 CH=CH2 ③
CH=CH2 ③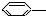 NO2
NO2
④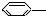 OH ⑤
OH ⑤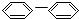 ⑥
⑥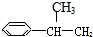
①
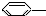 CH3 ②
CH3 ②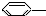 CH=CH2 ③
CH=CH2 ③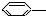 NO2
NO2④
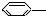 OH ⑤
OH ⑤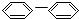 ⑥
⑥
| A. | ③④ | B. | ②⑤ | C. | ①②⑤⑥ | D. | ②③④⑤⑥ |
3.下列属于水解反应且正确的是( )
| A. | Fe3++3H2O═Fe(OH)3+3H+ | B. | Br-+H2O?HBr+OH- | ||
| C. | CO32-+2H2O?H2CO3+2OH- | D. | NH4++H2O?NH3•H2O+H+ |
 .
.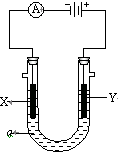 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: