题目内容
3.下列属于水解反应且正确的是( )| A. | Fe3++3H2O═Fe(OH)3+3H+ | B. | Br-+H2O?HBr+OH- | ||
| C. | CO32-+2H2O?H2CO3+2OH- | D. | NH4++H2O?NH3•H2O+H+ |
分析 A.水解反应是弱离子交换水电离出的氢离子或氢氧根离子形成弱电解质的过程,反应微弱可逆;
B.溴离子是强酸阴离子不能水解;
C.碳酸根离子是多元弱酸阴离子分步水解;
D.铵根离子是弱碱阳离子,结合水中氢氧根离子促进水电离,氢离子浓度增大;
解答 解:A.水解反应是弱离子交换水电离出的氢离子或氢氧根离子形成弱电解质的过程,反应微弱可逆,Fe3++3H2O?Fe(OH)3+3H+,故A错误;
B.溴离子是强酸阴离子不能水解,故B错误;
C.碳酸根离子是多元弱酸阴离子分步水解,水解离子方程式为:CO32-+H2O?HCO3-+OH-,故C错误;
D.铵根离子是弱碱阳离子,结合水中氢氧根离子促进水电离,氢离子浓度增大,水解离子方程式为:NH4++H2O?NH3•H2O+H+,故D正确;
故选D.
点评 本题考查了盐类水解的实质理解和离子方程式书写,掌握基础是解题关键,题目难度不大.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
13.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | CH3COOH | B. | Br2 | C. | SO2 | D. | NH4HCO3 |
14.常温下三氯化氮(NCl3)是一种淡黄色液体.以下关于NCl3的说法中,正确的是( )
| A. | 分子中 N-Cl键是非极性键 | B. | 分子中不存在孤对电子 | ||
| C. | 三氯化氮分子结构呈三角锥形 | D. | 因N-Cl 键键能大,它的沸点高 |
11.在一定温度下,向容积为1L的密闭容器中加入反应物A、B,发生可逆反应:A(s)+2B(g)?2C(g) 下列说法,属于该反应达到平衡标志的是( )
| A. | 容器内A、B、C的浓度之比为1:2:2 | |
| B. | 单位时间消耗0.2 mol/L B同时生成0.2 mol/L C | |
| C. | 容器内压强不随时间变化 | |
| D. | 容器内B的浓度不随时间变化 |
3.下列有机物的命名正确的是( )
| A. |  二溴乙烷 | B. | 2-甲基-3-乙基丁烷 | ||
| C. |  2-羟基丁烷 | D. |  2,3-二甲基-1,4-戊二烯 |
4.下列说法中正确的是( )
| A. | 1mol任何气体的体积均为22.4L | |
| B. | 32g氧气的体积约为22.4L | |
| C. | 标准状况下,18g水的体积是22.4L | |
| D. | 标准状况下,1mol任何气体的体积都约为22.4L |
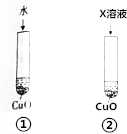 氧化铜可溶于稀硫酸,某同学为探究稀硫酸中的哪种粒子(H2O、H+、SO42-)使氧化铜溶解设计了如下实验.
氧化铜可溶于稀硫酸,某同学为探究稀硫酸中的哪种粒子(H2O、H+、SO42-)使氧化铜溶解设计了如下实验.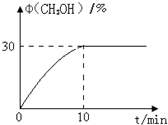 CO2加氢合成甲醇的技术,对减少温室气体排放和减缓燃料危机具有重要意义,发生的主要反应如下:CO2(g)+3H2(g)═CH3OH(g)+H2O(g).回答下列问题:
CO2加氢合成甲醇的技术,对减少温室气体排放和减缓燃料危机具有重要意义,发生的主要反应如下:CO2(g)+3H2(g)═CH3OH(g)+H2O(g).回答下列问题: