题目内容
4.NA为阿伏加德罗常数,下列说法正确的是( )| A. | 标准状况下,11.2L的己烷所含的分子数为0.5NA | |
| B. | 28g乙烯在氧气中完全燃烧消耗氧气分子的数目为3NA | |
| C. | 1mol甲基(-CH3)所含的电子总数为10NA | |
| D. | 分子式为C2H6O中含有C-H(碳氢键)的数目为6NA |
分析 A、标况下己烷为液态;
B、求出乙烯的物质的量,然后根据1mol乙烯消耗3mol氧气来分析;
C、甲基中含9个电子;
D、C2H6O可能为乙醇,还可能为二甲醚.
解答 解:A、标况下己烷为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、28g乙烯的物质的量为1mol,而1mol乙烯消耗3mol氧气,故消耗3NA个氧气分子,故B正确;
C、甲基中含9个电子,故1mol甲基中含9NA个电子,故C错误;
D、C2H6O可能为乙醇,还可能为二甲醚,故C2H6O中含有的C-H键的个数不一定为6NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
15.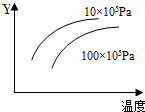 由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )
由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )
 由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )
由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )| A. | 正反应为一定为放热反应 | B. | 逆反应为体积缩小的反应 | ||
| C. | 升高温度,平衡常数K值减小 | D. | 该反应在一定条件下可自发进行 |
9.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4LH2O中所含原子总数为NA | |
| B. | 质量均为7.8 g的Na2S、Na2O2固体中含有的阴离子数均为0.1NA | |
| C. | 标准状况下,2.24 L Cl2通入足量H2O,转移的电子数均为0.1NA | |
| D. | 常温下,浓度为0.01mol/L的Na2CO3溶液中CO32-的数目为0.01 NA |
13.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | CH3COOH | B. | Br2 | C. | SO2 | D. | NH4HCO3 |
14.常温下三氯化氮(NCl3)是一种淡黄色液体.以下关于NCl3的说法中,正确的是( )
| A. | 分子中 N-Cl键是非极性键 | B. | 分子中不存在孤对电子 | ||
| C. | 三氯化氮分子结构呈三角锥形 | D. | 因N-Cl 键键能大,它的沸点高 |
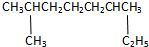 的系统命名是:2,6-二甲基辛烷
的系统命名是:2,6-二甲基辛烷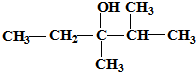 键线式是2,3-二甲基-3-戊醇
键线式是2,3-二甲基-3-戊醇 .
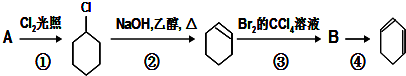
.
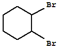 ;
; +Cl2 $\stackrel{光照}{→}$
+Cl2 $\stackrel{光照}{→}$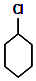 +HCl.
+HCl.