题目内容
19.下列关于浓硫酸的叙述正确的是( )| A. | 若浓硫酸不慎洒落在皮肤上应立即用干布拭去,再用大量水冲洗 | |
| B. | 可使蔗糖变黑,体现了浓硫酸的吸水性 | |
| C. | 常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓H2SO4不反应 | |
| D. | 可使胆矾变白,体现了浓硫酸的脱水性 |
分析 A.浓硫酸溶于水放出大量的热;
B.浓硫酸使蔗糖变黑表现脱水性;
C.浓硫酸与铝发生钝化反应;
D.浓硫酸使胆矾变白表现吸水性.
解答 解:A.浓硫酸溶于水放出大量的热,且具有腐蚀性,不能用水直接冲洗,应立即用干布拭去,故A正确;
B.浓硫酸使蔗糖变黑,蔗糖脱水、碳化,表现脱水性,故B错误;
C.浓硫酸与铝发生钝化反应,在表现生成一层致密的氧化膜,故C错误;
D.浓硫酸使胆矾变白表现吸水性,故D错误.
故选A.
点评 本题综合考查元素化合物知识,为高考常见题型,侧重于双基的考查,有利于培养学生良好的科学素养,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
9.以下说法不正确的是( )
| A. | 0.1 mol•L-1的盐酸与0.1 mol•L-1的氨水混合,若溶液显中性,则V(盐酸)<V(氨水) | |
| B. | 0.1 mol•L-1的醋酸与等浓度等体积NaOH反应后的溶液中,CH3COOH和CH3COO-浓度关系为:c(CH3COOH)+c(CH3COO-)=0.1 mol•L-1 | |
| C. | pH=3的盐酸与pH=11的氨水混合,若溶液显中性,则V(盐酸)>V(氨水) | |
| D. | 已知酸性:HCOOH>HCN,等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者大于后者 |
14.X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的化学式可表示为( )
| A. | XY | B. | XY2 | C. | XY4 | D. | X2Y3 |
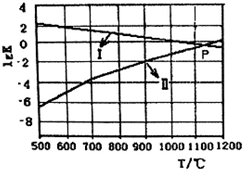 一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,可以减少SO2的排放,但产生的CO又会与CaSO4发生化学反应,从而降低脱硫效率.相关的热化学方程式如下:
一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,可以减少SO2的排放,但产生的CO又会与CaSO4发生化学反应,从而降低脱硫效率.相关的热化学方程式如下: