题目内容
9.向铁和氧化铁的混合物中加入足量的稀H2SO4,充分反应后生成FeSO4溶液,当生成的Fe2+和H2的物质的量之比为4:1时,被氧化的铁与被还原的铁的物质的量之比是( )| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 1:3 |
分析 铁和氧化铁的混合物中加入足量稀硫酸,充分反应后生成硫酸亚铁溶液,发生Fe+H2SO4═FeSO4+H2↑,Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,Fe+Fe2(SO4)3═3FeSO4,结合生成的Fe2+和H2的物质的量之比为4:1,设物质的量分别为4mol、1mol,结合反应方程式解答.
解答 解:铁和氧化铁的混合物中加入足量稀硫酸,充分反应后生成硫酸亚铁溶液,生成的Fe2+和H2的物质的量之比为4:1,设物质的量分别为4mol、1mol,
则Fe+H2SO4═FeSO4+H2↑,
1 1 1
Fe+Fe2(SO4)3═3FeSO4,
1 1 3
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,
1 1
显然被氧化的Fe为单质铁,其物质的量为1mol+1mol=2mol,
氧化铁的铁被还原,氧化铁为1mol,所以被还原的Fe为2mol,
所以被氧化的铁与被还原的铁离子物质的量之比为1:1,
故选A.
点评 本题考查氧化还原反应,为高考常见题型,题目难度中等,注意把握发生的氧化还原反应及习题中的信息是解答的关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
19.下列关于浓硫酸的叙述正确的是( )
| A. | 若浓硫酸不慎洒落在皮肤上应立即用干布拭去,再用大量水冲洗 | |
| B. | 可使蔗糖变黑,体现了浓硫酸的吸水性 | |
| C. | 常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓H2SO4不反应 | |
| D. | 可使胆矾变白,体现了浓硫酸的脱水性 |
17.25℃时,在某物质的溶液中,由水电离出的c(H+)=1×10-amol/L,下列说法正确的是( )
| A. | a<7时,水的电离受到抑制 | B. | a>7时,水的电离受到抑制 | ||
| C. | a<7时,溶液的pH一定为a | D. | a>7时,溶液的pH一定为14-a |
4.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径 A>B>D>C | B. | 原子序数 d>c>b>a | ||
| C. | 离子半径 C>D>B>A | D. | 元素的电负性 D>C>A>B |
14.同主族3种元素X、Y、Z,已知它们的最高价氧化物对应水化物的酸性HXO4>HYO4>HZO4,则下列判断正确的是( )
| A. | 原子半径X>Y>Z | B. | 气态氢化物稳定性 HX<HY<HZ | ||
| C. | 非金属性X>Y>Z | D. | 阴离子的还原性X->Y->Z- |
1.I2在KI溶液中存在下列平衡:I2 (aq)+I-(aq)?I3-(aq).测得不同温度下该反应的平衡常数如下表:( )
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1100 | 841 | 689 | 533 | 409 |
| A. | 反应I2 (aq)+I-(aq)?I3-(aq)的△H>0 | |
| B. | 其他条件不变,升高温度,溶液中c(I3-)减小 | |
| C. | 在上述平衡体系中加入苯,平衡不移动 | |
| D. | 25℃时向溶液中加入少量KI固体,平衡常数K大于689 |
18.历史上最早应用的还原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的是( )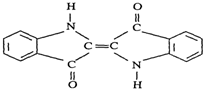

| A. | 靛蓝由碳、氢、氧、氮四种元素组成 | B. | 它的分子式是C12H10N2O2 | ||
| C. | 该物质是高分子化合物 | D. | 它是不饱和的有机物 |
19.Na和Na+两种粒子中,不相同的是( )
①核内质子数
②最内层电子数
③最外层电子数
④核外电子层数.
①核内质子数
②最内层电子数
③最外层电子数
④核外电子层数.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②③④ |
 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题