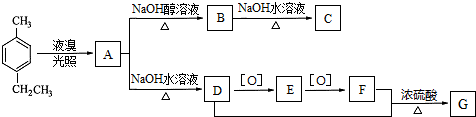
题目内容
下列物质的水溶液能导电,但属于非电解质的是( )
| A、HNO3 |
| B、Cl2 |
| C、SO2 |
| D、Na2O |
考点:电解质与非电解质
专题:物质的分类专题
分析:溶液能够导电,说明溶液中存在自由移动的带电离子;属于非电解质,说明该物质在水溶液和熔融状态下都不能导电,据此进行判断.
解答:
解:A.硝酸在水溶液中能够导电,且为化合物,硝酸属于电解质,故A错误;
B.氯气为单质,既不是电解质,也不是非电解质,故B错误;
C.二氧化硫的水溶液能够导电,由于导电离子不是二氧化硫本身电离的,所以二氧化硫为非电解质,故C正确;
D.氧化钠在熔融状态下能够导电,氧化钠为电解质,故D错误;
故选C.
B.氯气为单质,既不是电解质,也不是非电解质,故B错误;
C.二氧化硫的水溶液能够导电,由于导电离子不是二氧化硫本身电离的,所以二氧化硫为非电解质,故C正确;
D.氧化钠在熔融状态下能够导电,氧化钠为电解质,故D错误;
故选C.
点评:本题考查了溶液导电性、电解质与非电解质的判断,题目难度不大,注意掌握电解质与非电解质的概念及判断方法,明确溶液导电性实质.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知方程式 2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ/mol 则关于方程式 2H2O(l)=2H2(g)+O2(g)△H2=?的说法正确的是( )
| A、△H1=△H2 |
| B、该反应是吸热反应 |
| C、△H2=-571.6 kJ/mol |
| D、该反应可表示36g水蒸气分解时的热效应 |
下列离子方程式表达正确的是( )
| A、用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O |
| B、将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO- |
| C、向KHSO4溶液中加入Ba(OH)2溶液至所得溶液的pH=7 Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、向饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液Ca2++HCO3-+OH-=CaCO3↓++H2O |
元素在周期表中的位置反映了元素的原子结构和元素的性质,下列有关说法正确的是( )
| A、同一元素不可能既有金属性,又有非金属性 |
| B、第2周期主族元素的最高化合价都等于它所在的族序数 |
| C、短周期元素的简单离子,最外层并不都能达到8电子稳定结构 |
| D、同主族元素的原子,最外层电子数相同,因此化学性质也完全相同 |
下列叙述正确的是( )
| A、氯气的水溶液能导电,所以氯气属于电解质 |
| B、稀H2SO4溶液能导电,稀H2SO4是电解质 |
| C、由于NH3?H2O溶于水,而Ca(OH)2微溶于水,所以NH3?H2O是强电解质,Ca(OH)2是弱电解质 |
| D、硫酸钡难溶于水,但硫酸钡属于强电解质 |
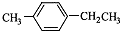 )是一种重要的有机原料,用该物质可合成其他物质.
)是一种重要的有机原料,用该物质可合成其他物质.