题目内容
已知方程式 2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ/mol 则关于方程式 2H2O(l)=2H2(g)+O2(g)△H2=?的说法正确的是( )
| A、△H1=△H2 |
| B、该反应是吸热反应 |
| C、△H2=-571.6 kJ/mol |
| D、该反应可表示36g水蒸气分解时的热效应 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:依据热化学方程式书写原则分析,反应系数变化,焓变随之变化,反应方向变化,焓变要变化符号;
A、互为可逆反应的两个反应过程焓变互为相反数;
B、焓变小于零的反应是放热的,大于零的反应是吸热的;
C、反应方向改变,焓变符号随之变化;
D、液态水的分解过程是吸热的过程.
A、互为可逆反应的两个反应过程焓变互为相反数;
B、焓变小于零的反应是放热的,大于零的反应是吸热的;
C、反应方向改变,焓变符号随之变化;
D、液态水的分解过程是吸热的过程.
解答:
解:A、反应方向改变,焓变符号随之变化,二者焓变焓变互为相反数,即△H1=-△H2,故A错误;
B、2H2O(l)=2H2(g)+O2(g)△H2=+571.6kJ?mol-1,△H2>0,该反应是吸热反应,故B正确;
C、反应方向改变,焓变符号随之变化,2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ?mol-1,则关于化学方程式:2H2O(l)=2H2(g)+O2(g)△H2=+571.6kJ?mol-1,故C错误;
D、△H2表示36g液态水分解时吸收的热量,故D错误;
故选B.
B、2H2O(l)=2H2(g)+O2(g)△H2=+571.6kJ?mol-1,△H2>0,该反应是吸热反应,故B正确;
C、反应方向改变,焓变符号随之变化,2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ?mol-1,则关于化学方程式:2H2O(l)=2H2(g)+O2(g)△H2=+571.6kJ?mol-1,故C错误;
D、△H2表示36g液态水分解时吸收的热量,故D错误;
故选B.
点评:本题考查了热化学方程式的书写方法和意义分析判断,题目较简单.

练习册系列答案
相关题目
苯酚和苯甲醇共同具有的化学性质是( )
| A、一定条件下能与Na反应放出H2 |
| B、与NaOH溶液加热能发生反应 |
| C、能与FeCl3溶液反应 |
| D、加入浓溴水能生成白色沉淀 |
下列实验操作不正确的是( )
| A、蒸发结晶时,应将蒸发皿中的NaCl溶液全部蒸干才停止加热 |
| B、蒸馏实验中,要在烧瓶中加入沸石或碎瓷片,以防止液体暴沸 |
| C、用托盘天平称量药品时,将砝码置于天平右盘 |
| D、用浓硫酸配制一定物质的量浓度的稀硫酸时,应冷却至室温再转移到容量瓶中 |
下列离子方程式书写正确的是( )
| A、铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑ | ||
| B、氢氧化钡与硫酸铜溶液混合:2OH-+Cu2+=Cu(OH)2↓ | ||
C、过量NaHCO3溶液和少量Ba(OH)2反应:2HCO
| ||
| D、石灰乳和盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
同时含有C12分子和C1-离子的物质是( )
| A、氯水 |
| B、液氯 |
| C、盐酸 |
| D、氯酸钾(KClO3) |
短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相同.下列化合物中同时存在离子键和非极性共价键的是( )
| A、Z2Y |
| B、X2Y2 |
| C、ZYX |
| D、Z2Y2 |
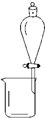
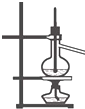
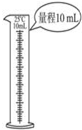
完成下列实验所选择的试剂、装置或仪器(部分夹持装置已略去)正确的是( )
| A | B | C | D | |
| 实 验 | 洗涤沉淀 | 用酒精提取溴水中的Br2 | 分离CCl4和苯的混合物 | 准确量取9.50mL水 |
| 装置或仪器 |  |
 |
 |
 |
| A、A | B、B | C、C | D、D |
某温度下将N2和H2充入一恒容的密闭容器中,发生可逆反应:N2+3H2?2NH3,某一时刻用下列各组内两种物质表示的该反应速率,其中正确的是( )
| A、v(N2)=O.01 mol?(L?s)-1,v(H2)=O.02 mol?(L?s)-1 |
| B、v(H2)=O.02 mol?(L?s)-1,v(NH3)=1.2 mol?(L?min)-1 |
| C、v(N2)=O.01 mol?(L?s)-1,v(NH3)=1.2 mol?(L?min)-1 |
| D、v(H2)=O.06 mol?(L?s)-1,v(NH3)=O.4 mol?(L?min)-1 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A、HNO3 |
| B、Cl2 |
| C、SO2 |
| D、Na2O |