题目内容
下列化学用语正确的是( )
A、聚丙烯的结构简式: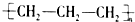 |
B、丙烷分子的比例模型: |
C、四氯化碳的电子式: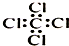 |
D、3-甲基-1-丁烯分子的键线式: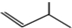 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.聚丙烯是丙烯通过加聚反应生成的,聚丙烯的主链含有2个碳原子;
B. 为球棍模型,比例模型主要体现出各原子相对体积大小;
为球棍模型,比例模型主要体现出各原子相对体积大小;
C.氯原子的最外层含有3对孤对电子没有标出;
D.该有机物为烯烃,根据烯烃的命名方法判断.
B.
 为球棍模型,比例模型主要体现出各原子相对体积大小;
为球棍模型,比例模型主要体现出各原子相对体积大小;C.氯原子的最外层含有3对孤对电子没有标出;
D.该有机物为烯烃,根据烯烃的命名方法判断.
解答:
解:A.聚丙烯是由丙烯不饱和的碳原子相互加成得到的,其结构简式为 ,故A错误;
,故A错误;
B. 为丙烷的球棍模型,丙烷的比例模型为:
为丙烷的球棍模型,丙烷的比例模型为: ,故B错误;
,故B错误;
C.氯原子未成键的孤对电子对未画出,四氯化碳是共价化合物,碳原子与氯原子之间形成1对共用电子对,电子式为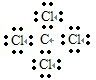 ,故C错误;
,故C错误;
D. 为烯烃的键线式,主链为1-丁烯,在3号C含有1个甲基,该烯烃正确的命名为:3-甲基-1-丁烯,故D正确;
为烯烃的键线式,主链为1-丁烯,在3号C含有1个甲基,该烯烃正确的命名为:3-甲基-1-丁烯,故D正确;
故选D.
 ,故A错误;
,故A错误;B.
 为丙烷的球棍模型,丙烷的比例模型为:
为丙烷的球棍模型,丙烷的比例模型为: ,故B错误;
,故B错误;C.氯原子未成键的孤对电子对未画出,四氯化碳是共价化合物,碳原子与氯原子之间形成1对共用电子对,电子式为
 ,故C错误;
,故C错误;D.
 为烯烃的键线式,主链为1-丁烯,在3号C含有1个甲基,该烯烃正确的命名为:3-甲基-1-丁烯,故D正确;
为烯烃的键线式,主链为1-丁烯,在3号C含有1个甲基,该烯烃正确的命名为:3-甲基-1-丁烯,故D正确;故选D.
点评:本题考查常见化学用语的判断,题目难度中等,注意掌握电子式、结构简式、球棍模型与比例模型等化学用语的表示方,选项C为易错点,注意甲烷与四氯化碳的电子式的区别.

练习册系列答案
相关题目
向恒温、恒容(2L)的密闭容器中充入2molX和一定量的Y,发生反应:2X(g)+Y(g)
2Z(g)△H=-197.74kJ?mol-1,4min后达到平衡,这时c(X)=0.2mol?L-1,且X与Y的转化率相等.下列说法错误的是( )
| 催化剂 |
| △ |
| A、达到平衡时,再充入1molX,该反应的△H保持不变 |
| B、用Y表示4min内的反应速率为0.1mol/(L?min) |
| C、4min后,若升高温度,平衡将向逆反应方向移动,平衡常数K增大 |
| D、再向容器中充入1molZ,达到新平衡,v(X):v(Y)=2:1 |
下列反应中,氯元素全部被氧化的是( )
| A、2P+3Cl2═2PCl3 | ||||
B、2NaCl
| ||||
| C、NaOH+HCl═NaCl+H2O | ||||
| D、2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O |
下列说法或表示正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定 |
| C、稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ |
| D、在101kPa时,H2燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol,则H2在101kPa时的燃烧热为571.6kJ/mol |
用水处理金属钠与碳化钙的混合物,有气体放出,此气体在催化剂作用下恰好完全反应,生成另一种气体A.气体A完全燃烧时,需要3.5倍体积的氧气,则金属钠与碳化钙的物质的量之比是( )
| A、2:1 | B、1:2 |
| C、4:1 | D、1:4 |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、64g SO2含有氧原子数为NA |
| B、物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数为NA |
| C、标准状况下,22.4L CCl4的分子数为NA |
| D、常温常压下,14g N2含有分子数为0.5NA |