题目内容
下列反应中,氯元素全部被氧化的是( )
| A、2P+3Cl2═2PCl3 | ||||
B、2NaCl
| ||||
| C、NaOH+HCl═NaCl+H2O | ||||
| D、2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O |
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应中氯元素全部被氧化,说明氯元素全部失电子化合价升高,发生氧化反应,据此分析解答.
解答:
解:A.该反应中Cl元素化合价由0价变为-1价,所以氯元素得电子化合价降低,全部被还原,故A错误;
B.该反应中Cl元素化合价由-1价变为0价,所以Cl元素失电子化合价升高,全部被氧化,故B正确;
C.该反应中没有电子转移,所以不是氧化还原反应,属于复分解反应,故C错误;
D.该反应中Cl元素化合价由0价变为-1价、+1价,所以Cl元素被氧化、被还原,故D错误;
故选B.
B.该反应中Cl元素化合价由-1价变为0价,所以Cl元素失电子化合价升高,全部被氧化,故B正确;
C.该反应中没有电子转移,所以不是氧化还原反应,属于复分解反应,故C错误;
D.该反应中Cl元素化合价由0价变为-1价、+1价,所以Cl元素被氧化、被还原,故D错误;
故选B.
点评:本题考查氧化还原反应,侧重考查基本概念,明确概念内涵是解本题关键,知道常见元素化合价.

练习册系列答案
相关题目
下列有关氯水的表述不正确的是( )
| A、向氯水中加入碳酸钙粉末,能提高溶液中HClO的浓度 |
| B、氯水中含有7种微粒,其可以与AgNO3、FeBr2等多种物质反应 |
| C、蓝色石蕊试纸放入氯水中先变红后褪色 |
| D、氯水可以导电,说明氯气是电解质 |
下列有关金属腐蚀与防护的说法正确的是( )
| A、当镀锡铁制品的镀层破损时,锡层仍能对铁制品起保护作用 |
| B、纯银器表面在空气中渐渐变暗是因为发生了化学腐蚀 |
| C、可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| D、在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阴极的阳极保护法 |
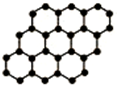 据物理学家组织网2012年4月16日报道,美国威斯康辛大学米尔沃基分校的科学家发现了一种全新的碳基材料一氧化石墨烯(GMO),其由碳家族的神奇材料石墨烯合成,石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如图),可由石墨剥离而成,具有极好的应用前景.下列说法正确的是( )
据物理学家组织网2012年4月16日报道,美国威斯康辛大学米尔沃基分校的科学家发现了一种全新的碳基材料一氧化石墨烯(GMO),其由碳家族的神奇材料石墨烯合成,石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如图),可由石墨剥离而成,具有极好的应用前景.下列说法正确的是( )| A、石墨烯与石墨互为同位素 |
| B、0.12g石墨烯中含有6.02×1022个碳原子 |
| C、石墨烯是一种有机物 |
| D、石墨烯中的碳原子间以共价键结合 |
Na2S2O3可用作纺织工业氯气漂白布匹后的“脱氯剂”:4C12+Na2S2O3+5H2O=2NaCl+2H2SO4+6HCl,有关该反应的叙述正确的是( )
| A、C12 是氧化剂 |
| B、H2SO4是氧化产物 |
| C、反应中S元素的价态降低 |
| D、反应中H2O被氧化 |
如图所示与对应的叙述相符的是( )
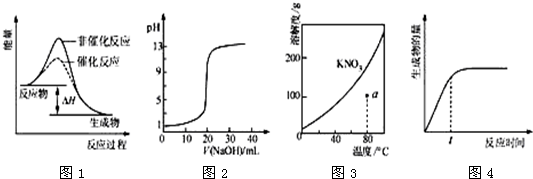

| A、图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B、图2表示0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1CH3COOH溶液所得到的滴定曲线 |
| C、图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| D、图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时v正>v逆 |
下列化学用语正确的是( )
A、聚丙烯的结构简式: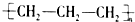 |
B、丙烷分子的比例模型: |
C、四氯化碳的电子式: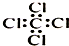 |
D、3-甲基-1-丁烯分子的键线式: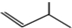 |
下列方程式正确的是( )
| A、表示甲醇燃烧热的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g);△H=-725KJ/mol |
| B、硫化钠溶液显碱性的原因:S2-+2H2O═H2S+2OH- |
| C、向硅酸钠溶液中通入足量的CO2:SiO32-+2CO2+3H2O=H4SiO4↓+2HCO3- |
| D、氧化亚铁溶于稀硝酸中:3FeO+NO3-+8H+=3Fe3++NO↑+4H2O |