题目内容
8.下列说法中错误的是( )| A. | 5 g 98%的硫酸(密度为1.84 g/cm3)与5 mL 18.4 mol/L硫酸的浓度是不同的 | |
| B. | 制成0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L(标准状况) | |
| C. | 0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 | |
| D. | 从1 L 1 mol/L的NaCl溶液中取出10 mL,其浓度仍是1 mol/L |
分析 A.根据c=$\frac{1000ρω}{M}$计算出98%的硫酸(密度为1.84 g/cm3)的浓度,然后进行判断;
B.根据n=cV计算出HCl的物质的量,然后根据V=nVm计算需要标况下HCl的体积;
C.根据n=cV计算出氯化钡的物质的量,然后计算出钡离子和氯离子的总物质的量,最后根据N=nNA计算出钡离子和氯离子总数;
D.溶液具有均一性,取出溶液的浓度不变.
解答 解:A.98%的硫酸(密度为1.84 g/cm3)的浓度为:$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,两溶液的浓度相等,故A错误;
B.0.5 L 10 mol/L的盐酸中含有HCl的物质的量为:10mol/L×0.5L=5mol,标况下5molHCl的体积为:22.4L/mol×5mol=112L,故B正确;
C.0.5 L 2 mol/L BaCl2溶液中含有氯化钡的物质的量为:2mol/L×0.5L=1mol,1mol氯化钡中含有1mol钡离子、2mol氯离子,总共含有3mol离子,含有Ba2+和Cl-总数为3×6.02×1023,故C正确;
D.从1L 1 mol/L的NaCl溶液中取出10 mL,取出溶液的物质的量浓度不变,其浓度仍是1 mol/L,故D正确;
故选A.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意溶液浓度与溶液体积无关,为易错点,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
18.下列化学用语表示正确的是( )
| A. | 氯化铁的化学式:FeCl | |
| B. | 乙烯的结构式:CH2=CH2 | |
| C. | Na2O的电子式: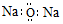 | |
| D. | KAl(SO4)2的电离方程式:KAl(SO4)2=K++Al3++2SO42- |
19.试根据碱金属元素性质的递变规律推测下列说法,其中不正确的是( )
| A. | Cs2CO3比CsHCO3稳定 | |
| B. | CsOH是一种强碱 | |
| C. | 可能存在Cs2O2 | |
| D. | Cs在金属活动性顺序表中排在K后面 |
16.已知CuCl2呈棕色,易溶于水及乙醇和丙酮,其水合物受热分解如下:2CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Cu(OH)2•CuCl2+2HCl↑+2H2O↑.则下列有关叙述中错误的是( )
| A. | CuCl2具有一定的氧化性 | |
| B. | 电解CuCl2水溶液时,阳极一定得到Cu单质 | |
| C. | Cu(OH)2•CuCl2 属于碱式盐 | |
| D. | 制备无水CuCl2时,需要在HCl气流中加热脱水 |
3.化学平衡常数(K)、电离常数(Ka、Kb)、水的离子积(Kw)、水解常数(Kh)、溶度积常数(Ksp)等是表示、判断物质性质的重要常数,下列说法正确的是( )
| A. | 化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关 | |
| B. | 降低温度时,弱酸和弱碱的电离常数(Ka、Kb)、水的离子积(Kw)均增大 | |
| C. | 向稀NaOH溶液中加入等体积等浓度的氯化镁和氯化铁混合溶液时,先产生红褐色沉淀,说明Ksp[Mg(OH)2]>Ksp[Fe(OH)3] | |
| D. | 室温下,Kh(CH3COONa)<Kh(NaCN),则等物质的量浓度时,CH3COOH的酸性比HCN弱 |
13.观察下列几个装置示意图,有关叙述正确的是( )
| A. | 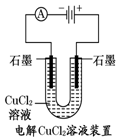 装置中阳极上析出红色固体 | |
| B. | 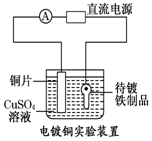 装置的待镀铁制品应与电源正极相连 | |
| C. | 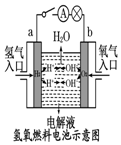 装置中外电路电子由a极流向b极 | |
| D. |  装置的阳极反应为:2H++2e-=H2↑ |
20.下列说法正确的是( )
| A. | 直径为20nm的纳米碳酸钙属于胶体 | |
| B. | 海水中含有钾元素,只需经过物理变化就可以得到钾单质 | |
| C. | 可溶性铁盐可用作净水剂 | |
| D. | 光导纤维是一种新型硅酸盐材料 |
17.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A. | Na2O、MgO、Fe3O4均为金属氧化物,并且都是碱性氧化物 | |
| B. | CH3COONa、CuSO4、NaOH、H2S水溶液均能导电,并且都是强电解质 | |
| C. | 赤铁矿、磁铁矿、黄铁矿、孔雀石都含有铁元素,并且都是常见的铁矿石 | |
| D. | HClO、H2SO4、HNO3均具有氧化性,并且都是氧化性酸 |
18.在给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
| A. | NH3$\stackrel{O_{2}}{→}$NO2 $\stackrel{H_{2}O}{→}$HNO3 | B. | SiO2$\stackrel{HCl}{→}$SiCl4$\stackrel{H_{2}/高温}{→}$Si | ||
| C. | Al2O3$\stackrel{NaOH(aq)}{→}$NaAlO2$\stackrel{CO_{2}}{→}$Al(OH)3 | D. | Na$\stackrel{O_{2}}{→}$ Na2O2$\stackrel{CO_{2}}{→}$Na2CO3 |