题目内容
17.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )| A. | Na2O、MgO、Fe3O4均为金属氧化物,并且都是碱性氧化物 | |
| B. | CH3COONa、CuSO4、NaOH、H2S水溶液均能导电,并且都是强电解质 | |
| C. | 赤铁矿、磁铁矿、黄铁矿、孔雀石都含有铁元素,并且都是常见的铁矿石 | |
| D. | HClO、H2SO4、HNO3均具有氧化性,并且都是氧化性酸 |
分析 A、依据和酸反应生成盐和水的氧化物为碱性氧化物分析;
B、强电解质包括强酸、强碱、大部分盐、活泼金属氧化物;
C、孔雀石主要成分为碱式碳酸铜;
D、稀H2SO4不是氧化性酸.
解答 解:A、Na2O、MgO、Fe3O4都能酸反应生成盐和水,属于碱性氧化物,故A正确;
B、H2S是弱酸,属于弱电解质,故B错误;
C、孔雀石主要成分为碱式碳酸铜,属于铜矿石,故C错误;
D、稀H2SO4不是氧化性酸,浓H2SO4是氧化性酸,故D错误;
故选A.
点评 本题考查了几个常见的概念,要注意对概念的准确把握.

练习册系列答案
相关题目
7.设阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 1.5g甲基(-CH3)所含有的电子数是9NA | |
| B. | 标准状况下,11.2L四氯化碳所含分子数为0.5 NA | |
| C. | 标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为5/22.4 NA | |
| D. | 常温常压下,1mol丙烷所含有的共价键数目为12NA |
8.下列说法中错误的是( )
| A. | 5 g 98%的硫酸(密度为1.84 g/cm3)与5 mL 18.4 mol/L硫酸的浓度是不同的 | |
| B. | 制成0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L(标准状况) | |
| C. | 0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 | |
| D. | 从1 L 1 mol/L的NaCl溶液中取出10 mL,其浓度仍是1 mol/L |
5.下列离子方程式正确的是( )
| A. | 向含nmolNH4Al(SO4)2的溶液中,逐滴加入含nmolNaOH的溶液:Al3++3OH-═Al(OH)3↓ | |
| B. | 向NaAlO2溶液中通入足量CO2气体:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| C. | 向溴水中通入SO2气体:SO2+Br2+2H2O═2H++SO42-+2HBr | |
| D. | 含2nmolNaOH的溶液和含nmolCa(HCO3)2的溶液混合OH-+Ca2++HCO3-═CaCO3↓+H2O |
2.制取甲烷的反应为C(s)+2H2(g)?CH4(g)△H>0,欲提高反应的速率和H2的转化率,可采用的措施为( )
| A. | 压缩容器体积 | B. | 降温 | ||
| C. | 增大C(s)的量 | D. | 恒温恒压时加入一定量H2 |
7.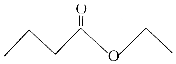 茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示,下列说法正确的是( )
茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示,下列说法正确的是( )
 茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示,下列说法正确的是( )
茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示,下列说法正确的是( )| A. | X难溶于乙醇 | |
| B. | X的分子式为C6H10O2 | |
| C. | 酒中的少量丁酸能抑制X的水解 | |
| D. | 分子式为C4H8O2且官能团与X相同的物质共有5种(不考虑立体结构) |
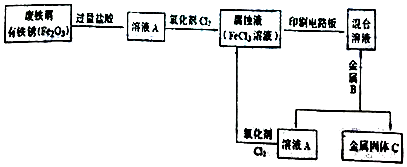
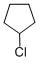 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$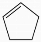 +NaCl+H2O.
+NaCl+H2O.