题目内容
4.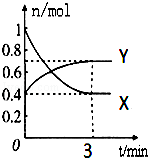 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4(g)(无色),如图所示.
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4(g)(无色),如图所示.(1)曲线X (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正)减慢,v(逆)减慢.(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则甲中反应更快.
(4)在0到3min中内N2O4的反应速率为0.05mol/(L•min).
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号)BCF;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
分析 (1)根据物质的量的变化量之比等于计量数之比分析;
(2)根据温度对反应速率的影响分析;
(3)根据反应速率之比等于化学计量数之比比较;
(4)根据v=$\frac{△c}{△t}$计算反应速率,结合图象计算相关物理量;
(5)根据可逆反应处于平衡状态时,正逆反应速率相等、组成不变等特征判断.
解答 解:(1)由方程式2NO2(g)(红棕色)?N2O4g)(无色),可知反应中NO2 的物质的量变化较大,则X表示NO2的物质的量随时间的变化曲线,故答案为:X;
(2)温度降低,正逆反应速率都减慢,故答案为:减慢;减慢;
(3)分别测得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),v(NO2)=2v(N2O4)=6mol•L-1•min-1=0.1mol/(L•s),则甲反应较快,
故答案为:甲;
(4)v(N2O4)=$\frac{\frac{0.7mol-0.4mol}{2L}}{3min}$=0.05mol/(L•min),故答案为:0.05mol/(L•min);
(5)A.v(NO2)=2v(N2O4),未体现正与逆的关系,故错误;
B.容器内压强不再发生变化,说明达平衡状态,故正确;
C.X的体积分数不再发生变化,说明达平衡状态,故正确;
D.容器内气体原子总数不再发生变化,从反应发生容器中原子总数就不变,所以不能作平衡状态的标志,故错误;
E. 只要反应发生就符合相同时间内消耗n mol的Y的同时生成2n mol的X,所以不一定达平衡状态,故错误;
F.相同时间内消耗n mol的Y的同时消耗2n mol的X,说明达平衡状态,故正确;
故选:BCF.
点评 本题考查较为综合,题目难度中等,注意把握化学反应速率以及化学平衡的基本知识即可解答该题.

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案| A. | I、Br、Cl | B. | Al、P、Si | C. | O、S、Na | D. | N、C、B |
| A. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm互为同位素 | |
| B. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的质量数相同 | |
| C. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm是同一种核素 | |
| D. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm是不同元素 |
| A. | 放电时溶液中的H+向负极移动 | |
| B. | 在放电时,正极发生的反应是 Pb(s)+SO42-(aq)=PbSO4(s)+2e- | |
| C. | 在放电时,该电池的负极材料是铅板 | |
| D. | 放电时负极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
| A. | 常温下,由水电离出的c(H+)=10-12mol/L,则溶液pH一定为12 | |
| B. | 已知H2C2O4是弱酸,其电离方程式为:H2C2O4?2H++C2O42- | |
| C. | 常温下,pH=10的氨水溶液中,由水电离出的c(H+)=10-10mol/L | |
| D. | 工业合成氨温度控制在500℃,目的是为了提高产率 |
| A. | 相同的式量 | B. | 相同的结构 | C. | 相同的通式 | D. | 相同的分子式 |

