题目内容
20. 一定条件下,反应2NH3(g)?N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示.下列说法正确的是( )
一定条件下,反应2NH3(g)?N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示.下列说法正确的是( )| A. | 压强:p1>p2 | B. | b、c两点对应的平衡常数:Kc>Kb | ||
| C. | a点:2v(NH3)正═3v(H2)逆 | D. | a点:NH3的转化率为$\frac{1}{3}$ |
分析 一定条件下,反应2NH3(g)?N2(g)+3H2(g),反应前后气体体积增大,图象分析可知温度升高N2的体积分数增大,说明反应正向为吸热反应,压强越大平衡逆向进行氮气体积分数减小,P1<P2,平衡常数随温度变化.
解答 解:一定条件下,反应2NH3(g)?N2(g)+3H2(g),反应前后气体体积增大,图象分析可知温度升高N2的体积分数增大,说明反应正向为吸热反应,压强越大平衡逆向进行氮气体积分数减小,P1<P2,平衡常数随温度变化.,
A.图象分析可知压强p1<p2 ,故A错误;
B.bc点是不同温度下的状态,温度越高平衡正向进行,平衡常数增大,则Kc>Kb ,故B正确;
C.a点是一定条件下的平衡状态,速率之比等于化学方程式计量数之比为正反应速率之比,3v(NH3)正═2v(H2)逆 能说明氢气正逆反应速率相同,故C错误;
D.设氨气起始量为2mol,折平衡后生成氮气物质的量为x,
2NH3(g)?N2(g)+3H2(g),
起始量(mol) 2 0 0
变化量(mol) 2x x 3x
平衡量(mol) 2-2x x 3x
图象可知氮气体积分数为0.1,则$\frac{x}{2+2x}$=0.1,
x=0.25mol,氨气转化率=$\frac{2×0.25}{2}$×100%=25%,故D错误;
故选B.
点评 本题考查了图象分析、影响反应速率、平衡的因素分析判断、化学平衡三行计算的应用,掌握基础是解题关键,题目难度中等.

| A. | $\frac{z}{12m}$ | B. | $\frac{12z}{m}$ | C. | $\frac{{N}_{A}}{m}$ | D. | $\frac{{N}_{A}}{z}$ |
(1)在一定条件下,可逆反应mA?nB+pC△H,达到平衡状态.
①若A、B、C都是气体,增大压强,平衡向正反应方向移动,则m大于n+p(填“大于”、“小于”或“等于”).
②其他条件不变,加热后A的质量减小,则反应△H大于0(填“大于”、“小于”或“等于”).
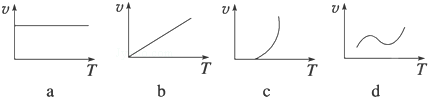
(2)某些金属氧化物(如FexOy)粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是c(填序号).
(3)一定温度下,发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H.已知该反应在不同温度下的平衡常数如表:
| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
①反应的△H<0(填“>”、“<”或“=”).
②T℃时,将FeO(s)和CO(g)各3.0mol加入10L的密闭容器中,反应达到平衡后,测得CO转化率为w1,c(CO2)=0.15mol•L-1,则温度T低于(填“高于”、“低于”或“等于”)1000,若此时保持其它条件不变再充入2.0mol CO(g),再达平衡时测得CO转化率为w2,则w1=w2(填“>”、“<”或“=”).
N2(g)+3H2(g)?2NH3(g)+Q(Q>0),
(1)该反应450℃的平衡常数>500℃时的平衡常数(填“>”、“<”或“=”).该反应达到平衡时混合气体的平均式量的范围是8.5<平均式量<17
(2)下列描述中能说明上述反应已达平衡的是BD
A、3V正(H2)=2V逆(NH3) B、容器中气体的平均分子量不随时间而变化
C、容器中气体的密度不随时间而变化 D、容器中气体的分子总数不随时间而变化
如上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol,计算从反应开始到平衡时,平均反应速率v(N2)为0.02mol/(L.min).
(3)下列研究目的和示意图相符的是C.
| A | B | C | D | |
| 研究目的 | 压强对反应的影响(P2>P1) | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 | 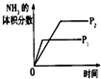 | 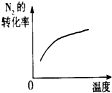 | 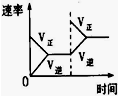 | 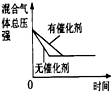 |
A、0.20mol/L B、0.16mol/L C、0.10mol/L D、0.05mol/L
在第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,则平衡向正反应方向移动(填“向正反应方向”“向逆反应方向”或“不”).
| A. | Ba2+、SO42-,Fe3+、K+ | B. | OH-、C1-、Na+ | ||
| C. | NH4+、NO3-、A13+、K+ | D. | HCO3-、SO42-、Na+、H+ |
| A. | Mg2+、Na+、SO42-、Cl- | B. | K+、CO32-、Cl-、NO3- | ||
| C. | Na+、K+、NO3-、SO42- | D. | NH4+、Na+、SO42-、NO3- |
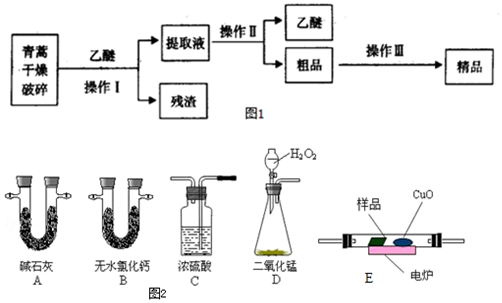
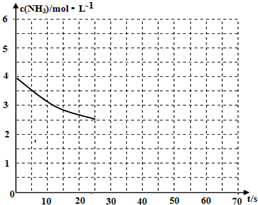 (2)①用氨气制取尿素[CO(NH2)]的反应为:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)△H<0.
(2)①用氨气制取尿素[CO(NH2)]的反应为:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)△H<0. 肼(N2H4)广泛用于火箭推进剂、有机合成及电池燃料.请回答下列问题:
肼(N2H4)广泛用于火箭推进剂、有机合成及电池燃料.请回答下列问题: