题目内容
7.设一个碳12C的原子的质量为m g,一个R原子的质量为z g,阿伏伽德罗常数为NA,则R的相对原子质量可表示为( )| A. | $\frac{z}{12m}$ | B. | $\frac{12z}{m}$ | C. | $\frac{{N}_{A}}{m}$ | D. | $\frac{{N}_{A}}{z}$ |
分析 相对原子质量=$\frac{1gR原子的质量}{C-12原子质量的\frac{1}{12}}$或数值上与NA个R原子的质量的数值相同,据此可计算出R的相对原子质量.
解答 解:一个12C原子的质量为mg,一个R原子的质量为zg,则R原子相对原子质量=$\frac{zg}{mg×\frac{1}{12}}$=$\frac{12z}{m}$,
若阿伏加德罗常数的值为NA,则R的摩尔质量为mNAg/mol,故其相对原子质量为mNA,
故选B.
点评 本题考查物质的量的计算,为高频考点,把握相对原子质量的计算方法及与阿伏伽德罗常数的关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
15.某兴趣小组甲设计了以下装置和方法测定空气中SO2含量.你认为可行的操作是B
| 序号 | A | B | C |
| 装置 | 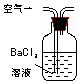 | 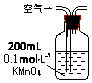 | 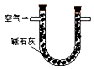 |
| 原理 | 通入V升空气,测定生成沉淀的质量 | 当KMnO4溶液刚好褪色时,测定通入空气的体积V | 通入V升空气,测定U型管增加的质量 |
2.根据如图提供的信息,下列所得结论不正确的是( )
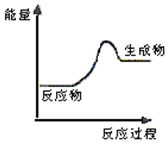

| A. | 该反应可能为吸热反应 | |
| B. | 该反应一定有能量转化成了生成物的化学能 | |
| C. | 反应物比生成物稳定 | |
| D. | 生成物的总能量高于反应物的总能量,反应不需要加热 |
12.下列化合物的分子中,所有原子都处于同一平面的有( )
| A. | 乙烷 | B. | 甲苯 | C. | CH2=CH-CN | D. | 异戊二烯 |
19.煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表:
试回答下列问题
(1)某温度下,上述反应达到平衡后,保持容器体积不变降低温度,平衡正向移动(填“正向移动”、“逆向移动”或“不移动”).
(2)在恒容绝热容器中,下列描述中能说明上述反应已达到平衡的是C
A、容器内混合气体分子总数不再发生变化
B、容器内混合气体的密度不再变化
C、$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$不再变化
D、单位时间内消耗18g H2O同时生成1mol CO2
(3)830℃时,在恒容密闭容器中发生上述反应,按表中的物质的量投入反应混合物,其中向正反应方向进行的有AD(选填字母序号).
(4)830℃时,在2L的密闭容器中加入4mol CO(g)和4mol H2O(g),2min达到平衡时,CO的转化率为50%,用CO表示的平均反应速率为0.5mol/(L•min).
已知:CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表:
| 温度℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(1)某温度下,上述反应达到平衡后,保持容器体积不变降低温度,平衡正向移动(填“正向移动”、“逆向移动”或“不移动”).
(2)在恒容绝热容器中,下列描述中能说明上述反应已达到平衡的是C
A、容器内混合气体分子总数不再发生变化
B、容器内混合气体的密度不再变化
C、$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$不再变化
D、单位时间内消耗18g H2O同时生成1mol CO2
(3)830℃时,在恒容密闭容器中发生上述反应,按表中的物质的量投入反应混合物,其中向正反应方向进行的有AD(选填字母序号).
| A | B | C | D | |
| n(CO2)/mol | 0 | 1 | 3 | 1 |
| n(H2)/mol | 0 | 2 | 2 | 1 |
| n(CO)/mol | 3 | 0.5 | 1 | 2 |
| n(H2O)/mol | 3 | 2 | 5 | 2 |
20. 一定条件下,反应2NH3(g)?N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示.下列说法正确的是( )
一定条件下,反应2NH3(g)?N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示.下列说法正确的是( )
 一定条件下,反应2NH3(g)?N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示.下列说法正确的是( )
一定条件下,反应2NH3(g)?N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示.下列说法正确的是( )| A. | 压强:p1>p2 | B. | b、c两点对应的平衡常数:Kc>Kb | ||
| C. | a点:2v(NH3)正═3v(H2)逆 | D. | a点:NH3的转化率为$\frac{1}{3}$ |