题目内容
15.化学理论在元素单质及其化合物反应中应用广泛.(1)在一定条件下,可逆反应mA?nB+pC△H,达到平衡状态.
①若A、B、C都是气体,增大压强,平衡向正反应方向移动,则m大于n+p(填“大于”、“小于”或“等于”).
②其他条件不变,加热后A的质量减小,则反应△H大于0(填“大于”、“小于”或“等于”).
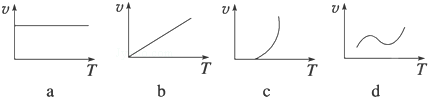
(2)某些金属氧化物(如FexOy)粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是c(填序号).
(3)一定温度下,发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H.已知该反应在不同温度下的平衡常数如表:
| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
①反应的△H<0(填“>”、“<”或“=”).
②T℃时,将FeO(s)和CO(g)各3.0mol加入10L的密闭容器中,反应达到平衡后,测得CO转化率为w1,c(CO2)=0.15mol•L-1,则温度T低于(填“高于”、“低于”或“等于”)1000,若此时保持其它条件不变再充入2.0mol CO(g),再达平衡时测得CO转化率为w2,则w1=w2(填“>”、“<”或“=”).
分析 (1)①增大压强,平衡向着方程式的系数减小的方向移动;
②升高温度,化学平衡向着吸热方向进行;
(2)据通过加热引发铝热反应以及铝热反应为放热反应以及温度升高化学反应速率加快;
(3)①根据温度和平衡常数以及反应的吸放热之间的关系来回答;
②根据达到平衡后,c(CO2)=0.15mol•L-1,计算平衡常数结合温度越高平衡常数越小比较;反应前后气体体积不变,又FeO为固态,所以再充入2.0mol CO(g),建立的平衡是等效的,据此判断.
解答 解:(1)mA?nB+pC△H,达到平衡状态.
①若A、B、C都是气体,增大压强,平衡向方式的系数减小的方向移动,即向正反应方向移动,则m>n+p,故答案为:大于;
②其他条件不变,升高温度,化学平衡向着吸热方向进行,即加热后A的质量减小,则反应正向进行,△H>0,故答案为:大于;
(2)因通过加热引发铝热反应,所以开始速率为零,一旦反应,反应放热,温度不断升高,化学反应速率加快,故选:c;
(3)①该反应的K随着温度的升高而减小,所以反应释放热量,△H<0,故答案为:<;
②T℃时,将FeO(s)和CO(g)各3.0mol加入10L的密闭容器中,
FeO(s)+CO(g)?Fe(s)+CO2(g)
初始浓度:0.3 0
变化浓度:0.15 0.15
平衡浓度:0.15 0.15
K═$\frac{0.15}{0.15}$=1,大于1000℃的平衡常数,根据表格得温度降低平衡常数增大,所以温度T低于1000℃;此时保持其它条件不变再充入2.0mol CO(g),因为反应前后气体体积不变,又FeO为固态,所以建立的平衡是等效的,则再达平衡时测得CO转化率为w2=w1
故答案为:低于;=.
点评 本题是一道关于化学平衡常数的计算题,考查生化学平衡移动原理以及三行式的计算知识,属于综合知识的考查,难度中等.

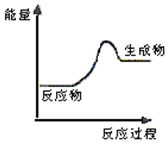
| A. | 该反应可能为吸热反应 | |
| B. | 该反应一定有能量转化成了生成物的化学能 | |
| C. | 反应物比生成物稳定 | |
| D. | 生成物的总能量高于反应物的总能量,反应不需要加热 |
(1)酸碱中和滴定--用标准盐酸滴定未知浓度的NaOH溶液.
①下列操作造成测定结果偏高的是AC
A.盛装未知液的锥形瓶先用蒸馏水洗过,再用未知液润洗
B.滴定终点读数时,俯视滴定管刻度,其他操作正确.
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,酸式滴定管尖嘴无气泡,滴定后有气泡
②该学生的实验操作如下:
A、用碱式滴定管取稀NaOH 25.00mL,注入锥形瓶中,加入酚酞做指示剂.
B、用待测定的溶液润洗碱式滴定管.
C、用蒸馏水洗干净滴定管.
D、取下酸式滴定管用标准的HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3cm处,再把滴定管固定好,调节液面至刻度“0”或“0”刻度以下.
E、检查滴定管是否漏水.
F、另取锥形瓶,再重复操作一次.
G、把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度.
滴定操作的正确顺序是(用序号填写)E→C→B→A→D→G→F
(2)氧化还原滴定--为了分析某残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行滴定,反应的离子方程式5Fe2++MnO${\;}_{4}^{-}$+8H+═5Fe3++Mn2++4H2O
①KMnO4标准溶液应盛装在酸式滴定管中(填“酸式”或“碱式”)
②某同学称取5.000g残留物,经预处理后在容量瓶中配制成100mL溶液,每次移取25.00mL试样溶液,用1.000×10-2 mol•L-1 KMnO4标准溶液滴定.四次实验消耗标准溶液的体积分别为19.90mL、20.00mL、20.10mL、20.60mL.计算该残留物中铁元素的质量分数是4.480%.
(3)沉淀滴定--滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶.
参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是C.
| 银盐 性质 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| 溶解度(mol•L-1) | 1.34×10-6 | 7.1×10-7 | 1.1×10-8 | 6.5×10-5 | 1.0×10-6 |
| A. | 平衡常数K增大 | B. | a+b<c+d | C. | X的转化率下降 | D. | Z的体积分数增加 |
 一定条件下,反应2NH3(g)?N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示.下列说法正确的是( )
一定条件下,反应2NH3(g)?N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示.下列说法正确的是( )| A. | 压强:p1>p2 | B. | b、c两点对应的平衡常数:Kc>Kb | ||
| C. | a点:2v(NH3)正═3v(H2)逆 | D. | a点:NH3的转化率为$\frac{1}{3}$ |
| A. | 蜡烛燃烧 | B. | 活性炭吸附冰箱中的异味 | ||
| C. | 分离液态空气制氧气 | D. | 海水晒盐 |
| A. | 1H和2H | B. | 14C和14N | C. | 37Cl和37Cl - | D. | 56Fe2+和56Fe3+ |
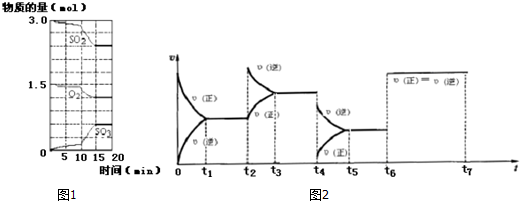
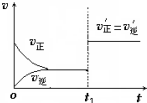 在其他条件不变的情况下,降低温度平衡向正反应方向移动,为放热反应(选填“吸热”、“放热”).如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是c(填写编号).
在其他条件不变的情况下,降低温度平衡向正反应方向移动,为放热反应(选填“吸热”、“放热”).如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是c(填写编号).