��Ŀ����
11�������������ĺ��������Ϊ��ɫ��״���壬�����ڱ�ͪ���ȷºͱ��У��ڼ״����Ҵ������ѡ�ʯ�����п��ܽ⣬��ˮ�м������ܣ��۵�Ϊ156��157�棬���ȶ��Բ�������Ǹ�Ч�Ŀ�űҩ����֪�����ѷе�Ϊ35�森����������ȡ�����صķ���֮һ������ȡԭ��Ϊ�����ģ���Ҫ�����ѽ�ȡ�������ͽ�ȡ�������ѽ�ȡ������Ҫ����Ϊ��ͼ1����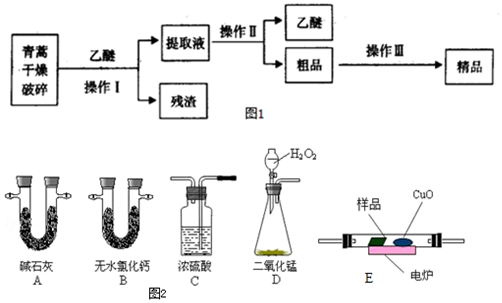
��ش��������⣺
��1����������и��������Ŀ�����������������ѵĽӴ��������������صĽ����ʣ�
��2������I��Ҫ�IJ���������Ҫ�У��ձ�����������©��������������������������������Ũ���ᾧ�����ˣ�
��3��ͨ����ȼ�յķ����ⶨ�л���ķ���ʽ������ȼ�����ڽ��л�����Ʒ�봿���ڵ�¯�����³��ȼ�գ����ݲ�Ʒ������ȷ���л������ɣ���ͼ2��ʾ������ȼ�շ�ȷ�������ط���ʽ��װ�ã�
�ٰ����������IJ�����Ϣ��װ�õ�����˳��Ӧ��DCEBA��ÿ��װ������һ�Σ���
�ڸ�ʵ��װ�ÿ��ܻ��������ɲⶨ������ƫ�ͣ��Ľ���������װ��A������һ����ֹ�����е�CO₂��ˮ��������A��װ�ã�
����������Ʒ������Ϊ28.2g���ú����Ľ����װ�ý������飬�Ƶ�A������66g��B������19.8g�����������ص����ʽ��C15H22O5��
��Ҫȷ�����л���ķ���ʽ��������֪������������Ʒ��Ħ��������
��4��ijѧ���������ص����ʽ���̽�����������ؼ��뺬��NaOH����̪��ˮ��Һ�У������ص��ܽ�����С�����Ȳ����裬�����ص��ܽ�����������Һ��ɫ��dz��˵����������D������ĸ��������ͬ�����ʣ�
A���Ҵ� B������ C�������� D������������
���� �����أ������ĺ��������Ϊ��ɫ��״���壬��ˮ�м������ܣ������ڱ�ͪ���ȷºͱ��У��ڼ״����Ҵ������ѡ�ʯ�����п��ܽ⣬��������и������飬�������ѽ�ȡͨ�����˵õ���ȡҺ�Ͳ�������ȡҺͨ������õ����Ѻʹ�Ʒ����Ʒͨ����95%�����ѣ�Ũ�����ᾧ�����˵õ���Ʒ��
��1������Ӵ����������Ӧ���ʺ��ܽ����ʣ�
��2���������Ƿ�������Һ��IJ���Ϊ����װ�ã��ݴ�ѡ����������Ϊ���ٲ�����Ľ��п������ó���װ�ã���������ͨ��������ȥ���ѣ����������Ϣ������֪�������أ������ĺ��������Ϊ��ɫ��״���壬�����ڱ�ͪ���ȷºͱ��У��ڼ״����Ҵ������ѡ�ʯ�����п��ܽ⣬��ˮ�м������ܣ��۵�Ϊ156��157�棬���ȶ��Բ���ѷе�Ϊ35����ڳ�ȥ����95%�����ѣ�Ũ���ᾧ���������ᴿ��ʵ�鷽����
��3����ʵ��ԭ���Dzⶨһ���������л�����ȫȼ��ʱ����CO2��H2O����������ȷ���Ƿ�����C��H��O�ĸ����ȣ�������ʽ���������O2�������ӣ���Ҫ�dz�H2O����ȷ��װ�õ������ǽ����ǰ�ᣬA�������ն�����̼���ⶨ���ɶ�����̼��������B��������ˮ���ⶨ����ˮ��������C���ڸ���ͨ��E�е�������D������ȡ��Ӧ�����������E���ڵ�¯����ʱ�ô���������������Ʒ������һ����̼��������ͭ��Ӧ���ɱ������ɶ�����̼�����ʿ�֪CuO�������ǰ��л��ﲻ��ȫȼ�ղ�����COת��ΪCO2���ݴ˶Ը�װ�ý�������
��װ��A�Ϳ���ֱ�ӽӴ���ʹ������̼��ˮ��������Ӱ��ⶨ�����
�۸���һ����̼��������ͭ��Ӧ���ɱ������ɶ�����̼�����ʿ�֪CuO�������ǰ��л��ﲻ��ȫȼ�ղ�����COת��ΪCO2��
�����и�ʵ�鷽��ֻ�ܻ���л����ʵ��ʽ��Ҫȷ���л���ķ���ʽ����Ҫ֪���л������Է���������Ħ��������
��4��������������ˮ����������������Һ��ˮ�Ⲣ�����������ƽ����жϣ�
��� �⣺��1����������и��������Ŀ�����������������ѵĽӴ��������������صĽ����ʣ�
�ʴ�Ϊ���������������ѵĽӴ��������������صĽ����ʣ�
��2�����������ڷ�������Һ�壬����ù��˵ķ������룬ѡ��������Ϊ�ձ�����������©����Ϊ���ٲ�����Ľ��п������ó���װ�ã������������ڷ������ѣ���������ķ������������Ǽ�95%�����ѣ�Ũ�����ᾧ���������ᴿ��ʵ�鷽����
�ʴ�Ϊ��©��������Ũ���ᾧ�����ˣ�
��3����D�����ɵ������к���ˮ������Ӧ��ͨ��C�е�Ũ��������E�е�¯����ʱ�ô�������������Ʒ�����ɶ�����̼��ˮ������һ����̼���ɣ���E��CuO����CO��һ����Ӧ���ɶ�����̼��Ȼ��ֱ�ͨ��B������ˮ����A�����ն�����̼���У����ݲ���������ƶ��л������ɣ��������������������������ѡ�õ�����˳��Ӧ�ǣ�D��C��E��B��A��
�ʴ�Ϊ��DCEBA��
�ڸ�ʵ��װ�ÿ��ܻ��������ɲⶨ������ƫ�ͣ��Ľ���������װ��F������һ����ֹ�����е�CO₂��ˮ��������A��װ�ã�
�ʴ�Ϊ����װ��A������һ����ֹ�����е�CO₂��ˮ��������A��װ�ã�
��A����������66gΪ������̼���������ɵ�̼Ԫ�ص�������66g��$\frac{12}{44}$=18g��
B����������19.8g��ˮ���������ɵ���Ԫ�ص�������19.8g��$\frac{2}{18}$=2.2g��
�Ӷ����Ƴ�����Ԫ�ص�����Ϊ��28.2-18-2.2=8g��
�����ʽΪCXHYOZ����
X��Y��Z=$\frac{18}{12}$��$\frac{2.2}{1}$��$\frac{8}{16}$=15��22��5�������ʽΪC15H22O5��
�ʴ�Ϊ��C15H22O5��
��������ɲ��������ܹ���������л����ʵ��ʽ��Ҫȷ���л���ķ���ʽ����Ҫ֪���л������Է���������Ħ�����������ʽ��n��������Ħ��������ֵ������õ�����ʽ��
�ʴ�Ϊ����Ʒ��Ħ��������
��4��������������ˮ����������������Һ��ˮ�Ⲣ�����������ƽ�������֪���������к�����������ѡD��
�ʴ�Ϊ��D��
���� ���⿼���Ϊ�ۺϣ��漰���ʵķ��롢�ᴿ�Լ����ʵ�������ؼ��㣬����ѧ���ķ�����ʵ�������Ŀ��飬��Ŀ��Ϊ������ע��������ʵ������Լ����������ʵ�����������Ŀ���еȣ�

 �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д� �¸��̵�ѧϵ�д�
�¸��̵�ѧϵ�д� ����ͬѧһ����ʦȫ�źþ�ϵ�д�
����ͬѧһ����ʦȫ�źþ�ϵ�д���֪��CO��g��+H2O��g��?H2��g��+CO2��g����ƽ�ⳣ�����¶ȵı仯�����
| �¶ȡ� | 400 | 500 | 830 | 1 000 |
| ƽ�ⳣ��K | 10 | 9 | 1 | 0.6 |
��1��ij�¶��£�������Ӧ�ﵽƽ���������������併���¶ȣ�ƽ�������ƶ���������ƶ������������ƶ������ƶ�������
��2���ں��ݾ��������У�������������˵��������Ӧ�Ѵﵽƽ�����C
A�������ڻ����������������ٷ����仯
B�������ڻ��������ܶȲ��ٱ仯
C��$\frac{c��C{O}_{2}��•c��{H}_{2}��}{c��CO��•c��{H}_{2}O��}$���ٱ仯
D����λʱ��������18g H2Oͬʱ����1mol CO2
��3��830��ʱ���ں����ܱ������з���������Ӧ�������е����ʵ���Ͷ�뷴Ӧ��������������Ӧ������е���AD��ѡ����ĸ��ţ���
| A | B | C | D | |
| n��CO2��/mol | 0 | 1 | 3 | 1 |
| n��H2��/mol | 0 | 2 | 2 | 1 |
| n��CO��/mol | 3 | 0.5 | 1 | 2 |
| n��H2O��/mol | 3 | 2 | 5 | 2 |
��1������к͵ζ�--�ñ�����ζ�δ֪Ũ�ȵ�NaOH��Һ��
�����в�����ɲⶨ���ƫ�ߵ���AC
A��ʢװδ֪Һ����ƿ��������ˮϴ��������δ֪Һ��ϴ
B���ζ��յ����ʱ�����ӵζ��̶ܿȣ�����������ȷ��
C����ʽ�ζ���������ˮϴ����δ�ñ�������ϴ
D���ζ�ǰ����ʽ�ζ��ܼ��������ݣ��ζ���������
�ڸ�ѧ����ʵ��������£�
A���ü�ʽ�ζ���ȡϡNaOH 25.00mL��ע����ƿ�У������̪��ָʾ����
B���ô��ⶨ����Һ��ϴ��ʽ�ζ��ܣ�
C��������ˮϴ�ɾ��ζ��ܣ�
D��ȡ����ʽ�ζ����ñ���HCl��Һ��ϴ����Һע��ζ��̶ܿȡ�0������2��3cm�����ٰѵζ��̶ܹ��ã�����Һ�����̶ȡ�0����0���̶����£�
E�����ζ����Ƿ�©ˮ��
F����ȡ��ƿ�����ظ�����һ�Σ�
G������ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬���µζ���Һ�����ڿ̶ȣ�
�ζ���������ȷ˳���ǣ��������д��E��C��B��A��D��G��F
��2��������ԭ�ζ�--Ϊ�˷���ij����������Ԫ�صĺ������Ƚ�������Ԥ������ʹ��Ԫ�ػ�ԭ��Fe2+������KMnO4����Һ�����������½��еζ�����Ӧ�����ӷ���ʽ5Fe2++MnO${\;}_{4}^{-}$+8H+�T5Fe3++Mn2++4H2O
��KMnO4����ҺӦʢװ����ʽ�ζ����У����ʽ����ʽ����
��ijͬѧ��ȡ5.000g�������Ԥ������������ƿ�����Ƴ�100mL��Һ��ÿ����ȡ25.00mL������Һ����1.000��10-2 mol•L-1 KMnO4����Һ�ζ����Ĵ�ʵ�����ı���Һ������ֱ�Ϊ19.90mL��20.00mL��20.10mL��20.60mL������ò���������Ԫ�ص�����������4.480%��
��3�������ζ�--�ζ����ͱ��ζ����������ȵζ�����ָʾ��������������ܣ�
�ο��±��е����ݣ�����AgNO3�ζ�NaSCN��Һ����ѡ�õ�ָʾ����C��
| ���� ���� | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| ��ɫ | �� | dz�� | �� | ש�� | �� |
| �ܽ�ȣ�mol•L-1�� | 1.34��10-6 | 7.1��10-7 | 1.1��10-8 | 6.5��10-5 | 1.0��10-6 |
 һ�������£���Ӧ2NH3��g��?N2��g��+3H2��g���ﵽƽ��ʱN2������������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
һ�������£���Ӧ2NH3��g��?N2��g��+3H2��g���ﵽƽ��ʱN2������������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ѹǿ��p1��p2 | B�� | b��c�����Ӧ��ƽ�ⳣ����Kc��Kb | ||
| C�� | a�㣺2v��NH3�����T3v��H2���� | D�� | a�㣺NH3��ת����Ϊ$\frac{1}{3}$ |