题目内容
“活化分子”是衡量化学反应速率快慢的重要依据,下列有关说法不正确的是( )
| A、能够发生有效碰撞的分子一定是活化分子 |
| B、增大浓度,单位体积内活化分子数增加,化学反应速率增大 |
| C、加入反应物,使活化分子百分数增大,化学反应速率增大 |
| D、一般使用催化剂可以降低反应的活化能,增大活化分子百分数,增大化学反应速率 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:增大浓度、增大压强,均使活化分子数目增多;而升高温度、使用催化剂,均使活化分子百分数增多,以此来解答.
解答:
解:A.能够发生有效碰撞的分子,能量较高,一定是活化分子,故A正确;
B.增大反应物的浓度,可使单位体积内活化分子数增多,有效碰撞机会增大,则反应速率加快,故B正确;
C.加入反应物,可使单位体积内活化分子数增多,但活化分子百分数不变,故C错误;
D.加入催化剂,降低反应的活化能,使单位体积内活化分子百分数大大增加,加快反应速率,故D正确.
故选C.
B.增大反应物的浓度,可使单位体积内活化分子数增多,有效碰撞机会增大,则反应速率加快,故B正确;
C.加入反应物,可使单位体积内活化分子数增多,但活化分子百分数不变,故C错误;
D.加入催化剂,降低反应的活化能,使单位体积内活化分子百分数大大增加,加快反应速率,故D正确.
故选C.
点评:本题考查影响化学反应速率的因素,为高频考点,侧重活化分子与活化理论的考查,注意外因因素变化与活化分子数目、百分数变化的关系,题目难度中等.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
下列各溶液不能与铜发生反应的是( )
| A、浓盐酸 |
| B、浓H2SO4 |
| C、浓硝酸 |
| D、稀硝酸 |
在一定固定体积的真空容器中充入1molPCl5,200℃时发生下列反应PCl5(g)?PCl3(g)+Cl2(g),达到平衡后,其他条件不变,再充入1molPCl5下列说法错误的是( )
| A、平衡向正向移动 |
| B、重新达到平衡时PCl5转化率增大 |
| C、重新达到平衡后PCl3体积分数减小 |
| D、反应速率加快 |
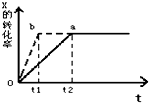 图中a曲线表示一定条件下的可逆反应:X(g)+Y(g)?2Z(g)+W(g);△H=QkJ/mol 的反应过程. 若使a曲线变为b曲线,可采取的措施是( )
图中a曲线表示一定条件下的可逆反应:X(g)+Y(g)?2Z(g)+W(g);△H=QkJ/mol 的反应过程. 若使a曲线变为b曲线,可采取的措施是( )| A、增大Y的浓度 |
| B、加入催化剂 |
| C、降低温度 |
| D、增大体系压强 |
PM2.5是灰霾天气的主要原因,是指大气中直径小于或等于2.5微米的颗粒物,也叫可入肺颗粒物,与肺癌、哮喘等疾病的发生密切相关,它主要来自化石燃料的燃烧(如机动车尾气、燃煤)等,下列说法不正确的是( )
| A、大力发展电动车,减少燃油汽车的尾气排放量 |
| B、燃煤时加入适量石灰石,可减少废气中SO2的排放量 |
| C、多环芳烃是强致癌物,能吸附在PM2.5的表面进入人体 |
| D、PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 |
pH、体积都相同的醋酸和硫酸,分别跟足量的碳酸钠溶液反应,在相同条件下,放出二氧化碳气体的体积是( )
| A、醋酸多 | B、硫酸多 |
| C、一样多 | D、无法比较 |
下列有关物质结构的表述正确的是( )
A、甲醇比例模型 |
B、CO2的电子式: |
| C、乙醛结构简式:CH3COH |
D、Cl-的结构示意图  |