题目内容
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、一定条件下,2.3g金属钠与氧气完全反应失电子数为0.1NA |
| B、常温常压下,氧气和臭氧(O3)的混合物32g中含有NA个氧原子 |
| C、1molOH- 中含有的电子数为9NA |
| D、0.1mol/L硫酸铝溶液中含有硫酸根的个数为0.3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、钠和水完全反应生成氢氧化钠和氢气,依据钠物质的量计算电子转移数;
B、依据氧元素守恒计算氧原子数;
C、氢氧根离子带一个负电荷是得到一个电子;
D、溶液体积不知不能计算微粒数;
B、依据氧元素守恒计算氧原子数;
C、氢氧根离子带一个负电荷是得到一个电子;
D、溶液体积不知不能计算微粒数;
解答:
解:A、钠和水完全反应生成氢氧化钠和氢气,依据钠物质的量计算电子转移数,2.3g金属钠物质的量为0.1mol,与氧气完全反应失电子数为0.1NA,故A正确;
B、氧元素守恒,氧气和臭氧(O3)的混合物32g中含有氧原子=
×NA=2NA个,故B错误;
C、氢氧根离子带一个负电荷是得到一个电子,1molOH- 中含有的电子数为10NA,故C错误;
D、溶液体积不知不能计算微粒数,故D错误;
故选A.
B、氧元素守恒,氧气和臭氧(O3)的混合物32g中含有氧原子=
| 32g |
| 16g/mol |
C、氢氧根离子带一个负电荷是得到一个电子,1molOH- 中含有的电子数为10NA,故C错误;
D、溶液体积不知不能计算微粒数,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析判断,主要是氧化还原反应电子转移,微粒结构分析,质量换算物质的量计算微粒数,题目较简单.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
下列叙述正确的是( )
| A、1L 0.1mol/L的碳酸钠溶液中C(Na+):C(CO32-)=2:1 |
| B、25℃时NaOH溶液中水的Kw大于100℃时NaCl溶液中水的Kw |
| C、中和体积相同pH相等的硫酸和醋酸溶液,消耗等物质的量浓度的NaOH溶液的体积:硫酸>醋酸 |
| D、25℃时,pH=8的0.1mol?L-1 NaX溶液中由水电离出的c(OH-)=10-6mol?L-1 |
用NA表示阿伏加德罗常数的值.下列说法正确是( )
| A、标准状况下,2.24L二氧化碳中含有共用电子对的数目为0.2NA |
| B、25℃时,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA |
| C、常温常压下,28g乙烯和丙烯的混合气体中含有碳原子的数目为2NA |
| D、0.1mol Cl2与足量铁粉反应转移电子的数目为0.3NA |
在一个固定容积的密闭容器中,可逆反应:mA(g)+nB(g)?pC(g)+qD(g)中,当m、n、p、q为任意正整数时,达到平衡的标志是( )
| A、体系压强不再发生变化 |
| B、反应速率vA:vB:vC:vD=m:n:p:q |
| C、容器内气体的密度不再改变 |
| D、各组分的物质的量浓度不再改变 |
下列事故处理方法正确的是( )
| A、凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
| B、制取并用排水法收集氧气结束后,应立即停止加热 |
| C、浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
| D、浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤 |
下列叙述不正确的是( )
| A、与28 gCO具有相同分子数的C2H4的质量一定是28 g |
| B、1 molAl3+含有的核外电子数为3NA |
| C、常温常压下,1 molL甲烷含有的原子数为5NA |
| D、1 L 1 mol?L-1醋酸溶液中CH3COO+的数目小于NA |

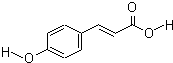 对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图:
对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图: