题目内容
用NA表示阿伏加德罗常数的值.下列说法正确是( )
| A、标准状况下,2.24L二氧化碳中含有共用电子对的数目为0.2NA |
| B、25℃时,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA |
| C、常温常压下,28g乙烯和丙烯的混合气体中含有碳原子的数目为2NA |
| D、0.1mol Cl2与足量铁粉反应转移电子的数目为0.3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量结合二氧化碳分子结构计算得到共用电子对数;
B、溶液体积不知不能计算微粒数;
C、乙烯和丙烯最简式相同为CH2,计算28gCH2中碳原子数;
D、氯气和铁反应生成氯化铁,电子转移依据反应的氯气计算;
| V |
| 22.4 |
B、溶液体积不知不能计算微粒数;
C、乙烯和丙烯最简式相同为CH2,计算28gCH2中碳原子数;
D、氯气和铁反应生成氯化铁,电子转移依据反应的氯气计算;
解答:
解:A、依据n=
计算物质的量=
=0.1mol,结合二氧化碳分子结构为O=C=O计算得到共用电子对数0.4NA,故A错误;
B、溶液体积不知不能计算微粒数,故B错误;
C、乙烯和丙烯最简式相同为CH2,计算28gCH2中碳原子数=
×NA=2NA,故C正确;
D、氯气和铁反应生成氯化铁,电子转移依据反应的氯气计算,0.1mol Cl2与足量铁粉反应转移电子的数目为0.2NA,故D错误;
故选C.
| V |
| 22.4 |
| 2.24L |
| 22.4L/mol |
B、溶液体积不知不能计算微粒数,故B错误;
C、乙烯和丙烯最简式相同为CH2,计算28gCH2中碳原子数=
| 28g |
| 14g/mol |
D、氯气和铁反应生成氯化铁,电子转移依据反应的氯气计算,0.1mol Cl2与足量铁粉反应转移电子的数目为0.2NA,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数分析应用,主要是气体摩尔体积的条件应用,质量换算物质的量计算微粒数,氧化还原反应电子转移计算,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
绿色化学己成为当前化学研究的热点和前沿,旨在从源头上消除污染,实现经济和社会可持续发展.而常温离子液体(ionic liquid)(也称常温熔融盐)以其优异的理化特性最有可能使上述理想变为现实.1914年报道的第一种离子液体硝酸乙基铵〔(C2H5NH3)NO3〕离子液体其熔点为12℃.已知C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是( )
| A、离子液体可以作为电池的电解质 |
| B、硝酸乙基铵水溶液呈碱性 |
| C、硝酸乙基铵水解的离子方程式表示为:C2H5NH3++H2O═C2H5NH2+H3O+ |
| D、相同温度下,相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液前者的pH值小 |
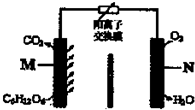 一种新型污水处理装置如图所示.该装置可利用一种微生物将有机废水的化学能直接转化为电能.下列说法中不正确的是( )
一种新型污水处理装置如图所示.该装置可利用一种微生物将有机废水的化学能直接转化为电能.下列说法中不正确的是( )| A、电池工作时H+从M极区移向N极区 |
| B、N极为正极,发生还原反应 |
| C、M极的电极反应式为:C6H12O6+6H2O-24e-═6CO2↑+24H+ |
| D、当N极消耗5.6L(标况下)气体时,则有2NA个H+通过离子交换膜 |
类推是化学学习与研究中常用的方法,下列类推的结论正确的是( )
| A、钠与氧气、水等反应时钠均作还原剂,则金属单质参与反应时金属单质均作还原剂 |
| B、铁能从硫酸铜溶液中置换出铜,则钠也能从硫酸铜溶液中置换出铜 |
| C、碳在少量氧气中燃烧生成CO、在过量氧气中燃烧生成CO2,则硫在少量氧气中燃烧生成SO2、在过量氧气中燃烧生成SO3 |
| D、铝粉在氧气中燃烧生成Al2O3,则铁丝在氧气中燃烧生成Fe2O3 |
下列实验基本操作(或实验注意事项)中,主要是从实验安全角度考虑的是( )
| A、实验剩余的药品一般不能放回原试剂瓶 |
| B、溶解时用玻璃棒搅拌 |
| C、可燃性气体点燃前必须验纯 |
| D、过滤时玻璃棒靠在三层滤纸处 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、一定条件下,2.3g金属钠与氧气完全反应失电子数为0.1NA |
| B、常温常压下,氧气和臭氧(O3)的混合物32g中含有NA个氧原子 |
| C、1molOH- 中含有的电子数为9NA |
| D、0.1mol/L硫酸铝溶液中含有硫酸根的个数为0.3NA |
R、X、Y、M、Z五种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素,R与Z的最外层电子数相同下列叙述正确的是( )
| A、Z与M形成的化合物中不可能含有非极性键 |
| B、对应氢化物的热稳定性:X>Y>M |
| C、单质的还原性:R>M>Y>X |
| D、X、Y、M、Z四种元素组成的离子化合物受热易分解 |
