题目内容
10.甲酸甲酯和甲酸的混合物中,氧元素的质量分数为65%,则碳元素的质量分数为( )| A. | 15% | B. | 20% | C. | 25% | D. | 30% |
分析 甲酸甲酯、甲酸分子中C、H原子数目之比均为1:2,则混合物中C、H元素质量之比为12:2=6:1,根据元素质量分数计算C、H元素总质量分数,再结合C、H质量之比计算碳元素质量分数.
解答 解:甲酸甲酯、甲酸分子中C、H原子数目之比均为1:2,则混合物中C、H元素质量之比为12:2=6:1,氧元素的质量分数为65%,则C、H元素总质量分数为1-65%=35%,故碳元素质量分数为35%×$\frac{6}{7}$=30%,
故选:D.
点评 本题考查混合物中元素质量分数计算,关键利用分子式确定C、H元素质量之比,掌握分子式进行的有关计算.

练习册系列答案
相关题目
1.已知常温下Ksp(AgCl)=1.8×l0-10,Ksp(AgBr)=5×10-13,下列有关说法错误的是( )
| A. | 在饱和AgCl、AgBr的混合溶液中c(Cl-)/c(Br-)=360 | |
| B. | 向AgCl悬浊液中滴加浓NaBr溶液会产生淡黄色沉淀 | |
| C. | AgCl在水中溶解度及Ksp均比在NaCl溶液中的大 | |
| D. | 向含有AgCl的饱和溶液中加入少量水后,c(Cl-)不变 |
5.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
| A. | 澄清石灰水、浓硫酸 | B. | KMnO4酸性溶液、浓硫酸 | ||
| C. | 溴水、浓硫酸 | D. | 浓硫酸、KMnO4酸性溶液 |
15.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: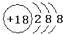 | |
| B. | HClO的结构式为:H-Cl-O | |
| C. | 氯化镁的电子式: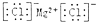 | |
| D. | 用电子式表示氯化氢分子的形成过程:H•+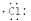 →H+ →H+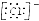 |
2.下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S;
②原子半径:K>Mg>S;
③酸性:H3PO4>H2SO4>HClO4;
④结合质子能力:OH->CH3COO->Cl-.
①热稳定性:H2O>HF>H2S;
②原子半径:K>Mg>S;
③酸性:H3PO4>H2SO4>HClO4;
④结合质子能力:OH->CH3COO->Cl-.
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ①④ |
19.放射性同位素${\;}_{92}^{238}$U的原子核内的中子数和核外电子数之差是( )
| A. | 54 | B. | 92 | C. | 146 | D. | 238 |
20.下列鉴别方法不可行的是( )
| A. | 用KMnO4(H+)溶液鉴别甲苯、丙烯、已烷 | |
| B. | 用溴水鉴别苯、丙烯、四氯化碳 | |
| C. | 用水鉴别乙醇、苯、四氯化碳 | |
| D. | 用NaOH溶液鉴别溴乙烷、甲苯、硝基苯 |


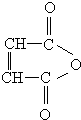 .
.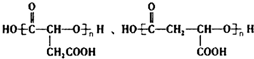 .
.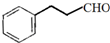 )与F的相对分子质量相同,其中满足下列条件的X的同分异构体有14种(含X本身).
)与F的相对分子质量相同,其中满足下列条件的X的同分异构体有14种(含X本身). 的最简合成线路.
的最简合成线路.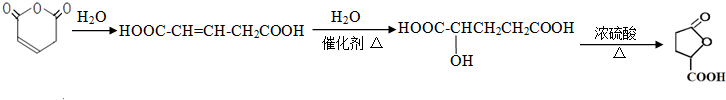 .
.