题目内容
19.放射性同位素${\;}_{92}^{238}$U的原子核内的中子数和核外电子数之差是( )| A. | 54 | B. | 92 | C. | 146 | D. | 238 |
分析 在原子的表示方法中元素符号左下角的数字为质子数,左上角的数字为质量数,并利用质量数=质子数+中子数、核外电子数等于核内质子数来分析.
解答 解:${\;}_{92}^{238}$U的质子数是92,质量数是238,中子数=质量数-质子数=238-92=146,所以故中子数与核外电子数之差为:146-92=54,故选A.
点评 本题考查原子的组成以及数量关系,明确质子数+中子数=质量数、核外电子数等于核内质子数是解答的关键.

练习册系列答案
相关题目
6.下列物质在给定条件下同分异构体数目正确的是( )
| A. | C4H10的属于烷烃的同分异构体有3种 | |
| B. | 分子组成是C5H10属于烯烃的同分异构体有6种 | |
| C. | 分子组成是C4H8O属于醛类的同分异构体有3种 | |
| D. | 结构为 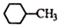 的物质的一溴代物有5种 的物质的一溴代物有5种 |
10.甲酸甲酯和甲酸的混合物中,氧元素的质量分数为65%,则碳元素的质量分数为( )
| A. | 15% | B. | 20% | C. | 25% | D. | 30% |
7.已知反应A2+B2═2AB,破坏1mol A2中的化学键消耗的能量为Q1 kJ,破坏1mol B2中的化学键消耗的能量为Q2 kJ,形成1mol AB中的化学键释放的能量为Q3 kJ,则下列说法正确的是( )
| A. | 若1mol A2和1 mol B2的总能量之和大于生成的1 mol AB的总能量,则反应放热 | |
| B. | 若1mol A2和1 mol B2的总能量之和小于生成的2 mol AB的总能量,则反应放热 | |
| C. | 若该反应为放热反应,则Q1+Q2<2Q3 | |
| D. | 若该反应为吸热反应,则Q1+Q2<Q3 |
4.下列有关氢化物的叙述中正确的( )
| A. | 气态氢化物稳定性:PH3>CH4 | |
| B. | HCl的电子式为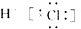 | |
| C. | D2O分子所有原子均达到最外层8e-稳定结构 | |
| D. | VIIA族元素中F的最高价氧化物对应水化物酸性最强 |
11.几种晶体的晶胞如图所示:
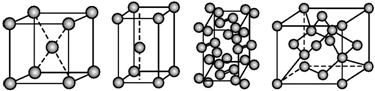
所示晶胞从左到右分别表示的物质正确的排序是( )

所示晶胞从左到右分别表示的物质正确的排序是( )
| A. | 碘、锌、钠、金刚石 | B. | 金刚石、锌、碘、钠 | C. | 钠、锌、碘、金刚石 | D. | 锌、钠、碘、金刚石 |
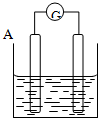 按要求回答下列问题:
按要求回答下列问题: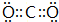 ,B与D形成的原子个数比为1:1的化合物乙的电子式是
,B与D形成的原子个数比为1:1的化合物乙的电子式是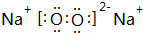 .
.