��Ŀ����
19�������ֳ�̼�������Ǻ�������ߵĵ��ʣ���ҵ�����ö�����̼�Ͱ�����һ�������ºϳ����أ��䷴Ӧ��Ϊ������������һ����2NH3��l��+CO2��g��?H2NCOONH4��l������������泥���H1=-330.0kJ•mol-1
�ڶ�����H2NCOONH4��l��?H2O��l��+CO��NH2��2��l����H2=+226.3kJ•mol-1
ijʵ��С��ģ�ҵ�Ϻϳ����ص���������һ���Ϊ0.5m3�ܱ�������Ͷ��4mol NH3��1mol CO2��ʵ���÷�Ӧ�и���ֵ����ʵ�����ʱ��ı仯��ͼ��ʾ��
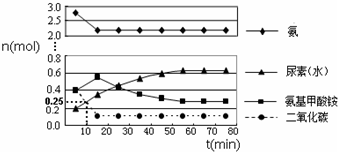
��1����֪�ܷ�Ӧ�Ŀ���������һ����������ϳ������ܷ�Ӧ�Ŀ����ɵڶ�����Ӧ�������ܷ�Ӧ���е���55minʱ����ƽ�⣮
��2����Ӧ���е�10minʱ���CO2�����ʵ�����ͼ��ʾ������CO2��ʾ�ĵ�һ����Ӧ������v��CO2��=1.5��10-4mol/��L•min����
��3������Ӧ��һ�������´ﵽƽ�⣬���ں��º������ٳ���һ��������He����CO��NH2��2��l�����������䣨����ӡ�������С�����䡱����
���� ��1����֪�ܷ�Ӧ�Ŀ���������һ�����������ͼ��仯���ƽ����жϣ���Ӧ�����������ݵ�һ���͵ڶ�����Ӧ������б�ʱȽϴ�С������ͼ�����������������������ƽ�⣻
��2������ͼ�����10����ʱ������̼���������ʵ�������ϻ�ѧ��Ӧ���ʸ�����м��㣻
��3�����¡��������ٳ���һ��������He����ƽ�ⲻ����Ӱ�죮
��� �⣺��1����ͼ���֪��15�������ң������Ͷ�����̼��Ӧ���ɰ�������狀��ٱ仯���������ǵ�һ����Ӧ������������������ټ�С���ﵽƽ�⣬�������ǵڶ�����Ӧ��������б�ʲ��ѿ����ڶ�����Ӧ����������֪�ܷ�Ӧ�Ŀ���������һ���������ʺϳ������ܷ�Ӧ�Ŀ����ɵڶ�������������ͼ�����55minʱ������������������ƽ�⣻
�ʴ�Ϊ������55��
��2������ͼ�������������̼�ٽ��е�10minʱ���ʵ���Ϊ0.25mol�����Դ�ʱ�ķ�Ӧ����Ϊ=$\frac{\frac{1mol-0.25mol}{500L}}{10min}$=1.5��10-4mol/��L•min����
�ʴ�Ϊ��1.5��10-4mol/��L•min����
��3�����¡��������ٳ���һ��������He����ƽ�ⲻ����Ӱ�죬��CO��NH2��2��l�����������䣬
�ʴ�Ϊ�����䣮
���� ���⿼�黯ѧƽ���Ӱ�����ط�������ѧ��Ӧ���ʵ�Ӱ�������жϣ�ͼ�������Ӧ�Ľ��г̶ȣ���Ŀ�Ѷ��еȣ�

 ������ϵ�д�
������ϵ�д���֪��
��MnO4-�����Ի����µĻ�ԭ������Mn2+
ʵ����Ʒ���������Թܣ����ɸ�������ͷ�ιܡ�100mL����ƿ��250mL����ƿ��10mL��Ͳ��������ƽ�����������ձ���ҩ��
��1��0.10mol/L H2C2O4��Һ�����ƣ�
ʵ����������100mL 0.10mol/L H2C2O4��Һ����Ҫ��ȡ���ᾧ�壨H2C2O4•2H2O��1.3 g����ȷ��0.1g����ʵ������Ҫ�õ��IJ��������У����������ձ�����ͷ�ιܺ�100mL����ƿ��
��2����Ӧ�����ʱ仯��̽����
��1�ź�2���Թ��зֱ����2mL0.10mol/L H2C2O4��Һ����1���Թ��м��������̹��壮Ȼ������֧�Թ��м���4mL 0.010mol/L KMnO4��Һ�ͼ���ϡ���ᣮ���������ʾ��
| �Թ�1 | �Թ�2 | |
| ʵ������ | ��ɫ�ܿ� | ��ɫ���� |
| ��ɫʱ��/s | 4�� | 31�� |
�ټ�ͬѧ���и�ʵ�黹ȱ�ٵ�ʵ�������ǣ������
��H2C2O4��Һ�����Ե�KMnO4��Һ��Ӧ�����ӷ���ʽΪ��5H2C2O4+2MnO4-+6H+=10CO2��+2Mn2++8H2O��
��ͬѧ�������ɫ�仯��ʱ�����������ĸ�ѡ��Ϊ���ݵ�C��
A����KMnO4��Һ�պýӴ�H2C2O4��Һ��ʼ����Һ���Ϻ�ɫ��Ϊ������ɫ�������֮�ڲ��ٳ����Ϻ�ɫΪֹ��
B����KMnO4��Һ�պýӴ�H2C2O4��Һ��ʼ����Һ����ɫ��Ϊ�Ϻ�ɫΪֹ��
C����KMnO4��Һ�Ӵ�H2C2O4��Һ��ʼ����Һ���Ϻ�ɫ��Ϊ������ɫΪֹ��
�ܼ�ͬѧ��Ϊ�÷�Ӧ��ɫ���������ԭ����Mn2+�����ڷ�Ӧ�����������ã��ӿ��˷�Ӧ���ʣ����Ǽ�ͬѧ�ó������������������������£���������ɼӿ컯ѧ��Ӧ���ʣ�
��3����ͬѧ�ͱ�ͬѧ�Ӽ�ͬѧ��ʵ��̽���еõ���ʾ������Ҳ�ֱ��������Ӱ�����Һ��ѧ��Ӧ�������ص��������ֿ���ԭ������Ϊ������������ֿ���ԭ���ǣ�I�÷�Ӧ�Ƿ��ȷ�Ӧ���¶����ߣ���Ӧ����������Һ��ɫ�ӿ� II�����������ᣬ���Դٽ�������������Һ�ķ�Ӧ��
| A�� | H2+CuO�TCu+H2O | B�� | 2Na2O2+2H2O�T4NaOH+O2�� | ||
| C�� | H2+Cl2�T2HCl | D�� | 2NaOH+Cl2�TNaCl+NaClO+H2O |
| A�� | NaH2PO4��ҺPH��7��������Һ�У�c��Na+����c��H2PO4-����c��H3PO4����c��HPO42-�� | |
| B�� | 0.1mol•L-1��NH4��2SO4��Һ��0.1mol•L-1NH3•H2O��Һ�������ϣ�c��NH4+��+c��H+��=2c��SO42-��+c��OH-�� | |
| C�� | 0.1mol•L-1CH3COONa��Һ��0.1mol•L-1CH3COOH��Һ�������ϣ�pH��7��c��CH3COOH����c��Na+����c��CH3COO-����c��H+�� | |
| D�� | 0.2mol•L-1NaHCO3��Һ��0.1mol•L-1Na2CO3��Һ�������ϣ�2c��Na+��=3c��CO32-��+3c��HCO3-��+3c��H2CO3�� |
| A�� | 10 mol | B�� | 11 mol | C�� | 12 mol | D�� | 13 mol |
| A�� | 8�� | B�� | 6�� | C�� | 4�� | D�� | 3�� |
 ��֪�������ȼ��Ϊ�£�N2H4����������Ϊ�������⣬������ֹ��������ѺϽ���ϣ���ش��������⣺
��֪�������ȼ��Ϊ�£�N2H4����������Ϊ�������⣬������ֹ��������ѺϽ���ϣ���ش��������⣺��1��N2H4��H2O2�����Ԫ���е�һ����������Ԫ����N��
��2���ѵ�ԭ��������22�����̬ԭ�ӵĺ�������Ų�ʽΪ[Ar]3d24s2��
��3��1molN2H4�������������Լ�����ĿΪ4NA��
��4��H2O2�����ֽ�ΪH2O��H2O�Ŀռ乹��ΪV�Σ�������ԭ�ӵ��ӻ��������Ϊsp3��
��5��H2S��H2O2����Ҫ�������������ʾ��
| ���� | �۵�/K | �е�/K | ˮ���ܽ�ȣ���״���� |
| H2S | 187 | 202 | ÿ��ˮ���ܽ�2.6L |
| H2O2 | 272 | 423 | ������Ȼ��� |
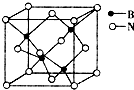
��6������þ�͵���������������زյ������β��ϣ������ܣ�����þ���������ƣ�����ڡ���С�ڡ�����
��7������������ľ�����ͼ��ʾ�����ھ��������ԭ�ӵ���λ��Ϊ4���������߳�Ϊa pm�����������������ܶ���$\frac{100}{{{N_A}{{��a��{{10}^{-10}}��}^3}}}$g•cm-3��ֻҪ������ʽ������٤������ΪNA����
| A�� | �����£�1 L 0.1 mol•L-1 ��NH4NO3��Һ�е�ԭ����Ϊ0.2NA | |
| B�� | ��״���£�2.24 L�����й��ۼ���ĿΪ1.9NA | |
| C�� | �����£�28.0 g��ϩ�Ͷ�ϩ�Ļ�������к��е�̼ԭ����Ϊ2NA | |
| D�� | ����Fe���״����22.4 L Cl2��ַ�Ӧ��ת�Ƶĵ�����Ϊ2NA |
