题目内容
14.镁是最轻的结构金属材料之一.金属镁性质活泼,能与空气中的O2、N2、CO2等反应,也能与沸水反应.其中,Mg与N2反应的产物Mg3N2与水反应的方程式为:Mg3N2+6H2O=3Mg(OH)2+2NH3↑.请回答下列问题:
(1)甲组学生研究Mg能在CO2气体中燃烧,并研究其产物.将镁条在空气中加热点燃后迅速插入盛放CO2气体的集气瓶中,观察到的现象是剧烈燃烧,发出耀眼白光,反应后在集气瓶内部附着白色粉末和黑色颗粒;;将集气瓶中加入足量的稀盐酸仍有黑色的固体未溶解,所以Mg在CO2气体中燃烧的化学反应方程式是2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO.
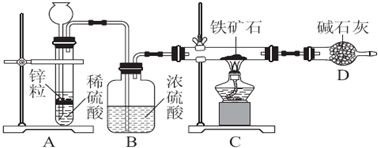
(2)乙组学生根据上述甲组实验,认为Mg能在NO2中燃烧,可能产物为MgO、N2和Mg3N2.通过如下实验装置来验证反应产物(夹持装置省略,部分仪器可重复使用).

已知:NO2气体能被NaOH吸收.
①乙组同学的装置中,依次连接的顺序为ABCBED(填字母序号);装置B的作用是在C的两侧防止水蒸气进入C中与产物 Mg3N2反应.
②确定产物中有N2生成的实验现象为D中试剂瓶中的水被气体压入烧杯中.
(3)设计实验证明:产物中存在Mg3N2取C中少量反应产物,加入到水中产生刺激性气味的气体,该气体可使湿润的红色石蕊试纸变蓝.
分析 (1)镁和二氧化碳在点燃条件下反应生成MgO和C,同时发出耀眼白光;
(2)①装置A:铜和浓硝酸制取二氧化氮,装置B:干燥二氧化氮,防止水蒸气干扰实验,在加热条件下将Mg和二氧化氮混合,然后再干燥气体,装置C:镁条和二氧化氮反应,装置D:排水法收集N2,装置E:吸收二氧化氮,然后用排水法收集N2;
②氮气不溶于水,如果有氮气,则能通过排水法收集到气体;
(3)氮化镁和水反应生成氢氧化镁和氨气,氨气能使湿润的红色石蕊试纸变蓝色.
解答 解:(1)镁和二氧化碳在点燃条件下反应生成MgO和C,同时发出耀眼白光,所以看到的现象是:剧烈燃烧,发出耀眼白光,反应后在集气瓶内部附着白色粉末和黑色颗粒,其中的C不溶于盐酸中,反应方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO.,
故答案为:剧烈燃烧,发出耀眼白光,反应后在集气瓶内部附着白色粉末和黑色颗粒;黑;2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO;
(2)①Mg能在NO2中燃烧,产物为Mg3N2、Mg0和N2,装置A中Cu与浓硝酸反应生成的气体NO2,用装置B干燥剂干燥,通入硬质玻璃管C与镁粉发生反应,然后再干燥气体,用E装置除去多余的NO2,装置D排水法收集N2,故连接装置的顺序为:BCBED,用装置B干燥剂干燥,通入硬质玻璃管C与镁粉发生反应,然后再干燥气体,装置B中的作用是在C的两侧防止水蒸气进入C中与产物Mg3N2反应,
故答案为:BCBED;在C的两侧防止水蒸气进入C中与产物 Mg3N2反应;
②氮气不溶于水,如果有氮气,则能通过排水法收集到气体,所以确定产物中有N2生成的实验现象为D中试剂瓶中的水被气体压入烧杯中,
故答案为:D中试剂瓶中的水被气体压入烧杯中;
(3)取C中少量反应后的固体产物,加入到水中产生有刺激性气味的气体,该气体能使湿润的红色石蕊试纸变成蓝色,证明产物中存在Mg3N2.
故答案为:取C中少量反应产物,加入到水中产生刺激性气味的气体,该气体可使湿润的红色石蕊试纸变蓝.
点评 本题考查了物质性质的实验探究,理解实验原理、掌握实验基本操作和镁及其化合物性质是解题关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| 实验 编号 | 实验目的 | 温度/℃ | 催化剂 质量/g | 反应物初始浓度 /10-3mol•L-1 | |
| H2 | I2 | ||||
| Ⅰ | 为以下实验作参照 | 457 | 0 | 7 | 9 |
| Ⅱ | ① | 420 | ② | 7 | 9 |
| Ⅲ | 探究催化剂对该反应速率的影响 | ③ | 10 | 7 | 9 |
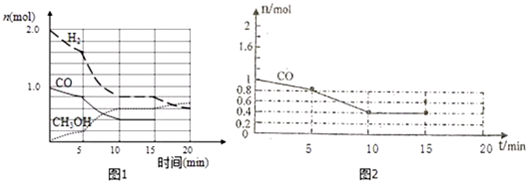
(2)实验Ⅰ中,I2的物质的量浓度(c)随时间(t)的变化如图所示.
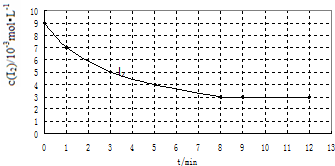
根据图中数据回答下列问题:
①在0~5min内反应的平均速率v(I2)=1×10-3mol•L-1•min-1.
②该温度下,反应的平衡常数K=$\frac{{c}^{2}(HI)}{c({H}_{2})×c({I}_{2})}$=48.(前空写表达式,后空写计算所得的数据)
③该同学还想用此反应研究压强对化学平衡移动的影响,请问能否达到实验目的?请说明原因.
不能(填“能”、不能”),原因是该反应前后气体计量数相等,平衡不受压强的影响.
| A. | Na、Mg、Al还原性依次增强 | |
| B. | HCl、PH3、H2S稳定性依次减弱 | |
| C. | NaOH、KOH、Ca(OH)2碱性依次减弱 | |
| D. | S2-、Cl-、K+、Ca2+离子半径依次减小 |
| A. | 1 L 1 mol•L-1的NaClO 溶液中含有ClO-的数目为NA | |
| B. | 常温常压下,4.6gCH3CH2OH中含有 6NA个C-H键 | |
| C. | 常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA |
| A. | 将2mol SO3气体通入一定密闭容器中,反应达到平衡后吸收Q kJ热量,则该反应的热化学方程式为 2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ•mol-1 | |
| B. | 向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:H++OH-=H2O | |
| C. | 以金属银为阳极电解饱和硫酸铜溶液:Cu2++2H2O=2Cu+O2↑+4H+ | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向1mL 0.1mol/LAgNO3溶液中滴加2滴0.1mol/LNaCl溶液,振荡后,再滴加2滴0.1mol/LKI溶液 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 加热盛有浓硫酸和可抽动铜丝的试管,并将产生的气体通入到品红溶液中 | 品红溶液褪色,且试管中只产生蓝色溶液 | 浓硫酸具有强氧化性 |
| C | 向丙烯醇(HOCH2CH=CH2)中滴入少量酸性高锰酸钾溶液 | 溶液紫红色褪去 | 丙烯醇中含有碳碳双键 |
| D | 碳酸钠溶液中滴加稀硫酸后,将产生的气体通入到硅酸钠溶液中 | 产生白色沉淀 | 非金属性:S>C>Si |
| A. | A | B. | B | C. | C | D. | D |