题目内容
11.某饱和酯A在酸性条件下水解得到羧酸B和醇C,B与C的分子式分别为C5HxOy和C3H8O,已知它们的相对分子质量的关系式为:M(A)+36=M(B)+2M(C),则A的可能结构有(不考虑立体异构)( )| A. | 8种 | B. | 6种 | C. | 4种 | D. | 3种 |
分析 某饱和酯A在酸性条件下水解得到羧酸B和醇C,B与C的分子式分别为C5HxOy和C3H8O,已知它们的相对分子质量的关系式为:M(A)+36=M(B)+2M(C),说明羧酸为饱和二元酸,分子式为C5H8O4,结构简式有4种:(HOOC)2CHCH2CH2COOH、HOOCCH2CHCOOHCH3、HOOCCH2CH2CH2COOH、CH3C(COOH)2CH3;丙醇(C3H8O)结构简式有2种:(CH3CH2CH2OH、CH3CHOHCH3,以此判断形成的酯的同分异构体的种类.
解答 解:某饱和酯A在酸性条件下水解得到羧酸B和醇C,B与C的分子式分别为C5HxOy和C3H8O,已知它们的相对分子质量的关系式为:M(A)+36=M(B)+2M(C),说明羧酸为饱和二元酸,分子式为C5H8O4,结构简式有4种:(HOOC)2CHCH2CH2COOH、HOOCCH2CHCOOHCH3、HOOCCH2CH2CH2COOH、CH3C(COOH)2CH3;丙醇(C3H8O)结构简式有2种:(CH3CH2CH2OH、CH3CHOHCH3,某饱和酯A的可能结构有4×2=8,故选A.
点评 本题考查同分异构体数目的判断,题目难度中等,明确醇的种类与羧酸的种类是解题的关键,注意掌握同分异构体的书写原则.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1. 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
(1)配制100mL 0.10mol/L NaOH标准溶液.
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作2~3次,记录数据如下.
①滴定达到终点的现象是最后一滴NaOH溶液滴入后,锥形瓶中溶液恰好出现红色,且半分钟内红色不褪去.
②根据上述数据,计算出该盐酸的浓度约为0.11mol/L(保留两位有效数字)
③下列操作(其他操作正确)会造成实验测定结果偏高的有DF.(多选扣分)
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、称量前NaOH固体中混有Na2CO3固体
E、配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F、碱式滴定管尖嘴部分有气泡,滴定后消失
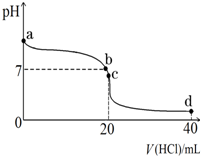
(3)室温下,若将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.
①NH3•H2O的电离方程式是NH3•H2O?NH4++OH-.
②b点所示溶液中的溶质是NH4Cl、NH3?H2O.
③c点所示溶液中,离子浓度从大到小的关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-),在该溶液中存在多种守恒关系,其中c(NH4+)+c(H+)=c(Cl-)+c(OH-)(用离子浓度表示).
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:(1)配制100mL 0.10mol/L NaOH标准溶液.
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作2~3次,记录数据如下.
| 实验编号 | NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 22.62 | 20.00 |
| 2 | 22.72 | 20.00 |
| 3 | 22.80 | 20.00 |
②根据上述数据,计算出该盐酸的浓度约为0.11mol/L(保留两位有效数字)
③下列操作(其他操作正确)会造成实验测定结果偏高的有DF.(多选扣分)
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、称量前NaOH固体中混有Na2CO3固体
E、配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F、碱式滴定管尖嘴部分有气泡,滴定后消失
(3)室温下,若将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.
①NH3•H2O的电离方程式是NH3•H2O?NH4++OH-.
②b点所示溶液中的溶质是NH4Cl、NH3?H2O.
③c点所示溶液中,离子浓度从大到小的关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-),在该溶液中存在多种守恒关系,其中c(NH4+)+c(H+)=c(Cl-)+c(OH-)(用离子浓度表示).
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 L 1 mol•L-1的NaClO 溶液中含有ClO-的数目为NA | |
| B. | 常温常压下,4.6gCH3CH2OH中含有 6NA个C-H键 | |
| C. | 常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA |
3.下列离子方程式或化学方程式与所述事实相符且正确的是( )
| A. | 将2mol SO3气体通入一定密闭容器中,反应达到平衡后吸收Q kJ热量,则该反应的热化学方程式为 2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ•mol-1 | |
| B. | 向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:H++OH-=H2O | |
| C. | 以金属银为阳极电解饱和硫酸铜溶液:Cu2++2H2O=2Cu+O2↑+4H+ | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
1.化学与科学研究、工农业生产、环境保护、日常生活等方面有广泛联系.下列有关说法中正确的是( )
| A. | 石灰石可用于炼铁、制水泥、制玻璃 | |
| B. | 使用苯代替酒精擦拭手机屏幕 | |
| C. | 同位素示踪法、红外光谱法都是科学家经常使用的研究化学反应历程的手段之一 | |
| D. | 针对H7N9禽流感的扩散情况,要加强环境、个人等的消毒预防,可选用含氯消毒剂、酒精、双氧水等作为消毒剂,这种处理方法符合绿色化学的核心 |