题目内容
1.为防止NO2污染空气,科学家寻求合适的化合物G和催化剂,以实现反应:NO2+G $\stackrel{催化剂}{?}$N2+H2O+nZ (未配平,n可以为0),上述反应式中的G不可能是( )| A. | CO | B. | NH3 | C. | H2O2 | D. | CH3CH2OH |
分析 可从质量守恒的角度分析,反应后生成H2O,则G中一定含有H元素.
解答 解:根据反应NO2+G--N2+H2O+nY,从质量守恒的角度分析,反应后生成H2O,则G中一定含有H元素,对比选项,只有CO不含有H元素,
故选A.
点评 本题考查氧化还原反应知识,为高频考点,着重于质量守恒定律的考查,注意从元素守恒的角度可快速分析.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
11.下列过程中涉及化学反应的是( )
| A. | 通过“扫描隧道显微镜”操纵原子“书写”文字 | |
| B. | 14C考古断代 | |
| C. | 煤焦油分馏得到苯及其同系物 | |
| D. | 粮食酿酒 |
12.化学与生产、生活和社会密切相关.下列说法正确的是( )
| A. | 用米汤检验碘盐中的碘 | |
| B. | 用热的烧碱溶液洗涤餐具上的油污 | |
| C. | “地沟油”禁止食用,但可用来制取肥皂 | |
| D. | 将洁厕灵与84消毒液混合使用,能更有效的起到洁具除垢和卫生消毒作用 |
9.为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如图.下列说法正确的是( )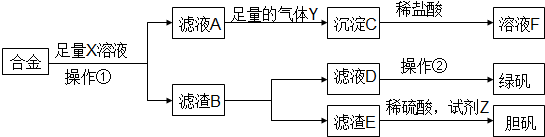

| A. | 溶液X为稀硫酸,气体Y为氨气 | |
| B. | 由溶液F获得溶质F固体的过程中,须控制条件防止其氧化和分解 | |
| C. | 使用足量稀硫酸时,试剂Z选用H2O2或适量HNO3均获得胆矾晶体 | |
| D. | 操作①为过滤,操作②为蒸发结晶、洗涤、干燥 |
6.如表为元素周期表的一部分,其中Q、X、Y、Z、W为短周期元素,Z元素原子的核电荷数为X元素的2倍.下列说法正确的是( )
| Q | X | ||
| Y | Z | W | |
| T |
| A. | X、Z、Y元素的原子半径及它们的气态氢化物的热稳定性均依次递增 | |
| B. | Y、Z、W元素在自然界中均能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | Q与氢元素形成的化合物中不存在非极性共价键 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,最高价氧化物对应水化物的化学式是H3TO4 |
13.在一定温度下,下列叙述不是可逆反应A(气)+3B(气)?2C(气)+2D(固)达到平衡的标志的是( )
①C的生成速率与C的分解速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④A、B、C的分压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦A、B、C、D的分子数之比为1:3:2:2.
①C的生成速率与C的分解速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④A、B、C的分压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦A、B、C、D的分子数之比为1:3:2:2.
| A. | ②⑦ | B. | ②⑤⑦ | C. | ①③④ | D. | ②⑤⑥⑦ |
10.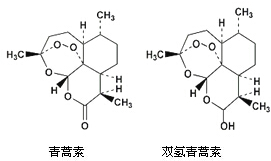 中国女药学家屠呦呦因创新性抗疟药青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖.颁奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.下列关于青蒿素和双氢青蒿素(结构如图)说法错误的是( )
中国女药学家屠呦呦因创新性抗疟药青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖.颁奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.下列关于青蒿素和双氢青蒿素(结构如图)说法错误的是( )
 中国女药学家屠呦呦因创新性抗疟药青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖.颁奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.下列关于青蒿素和双氢青蒿素(结构如图)说法错误的是( )
中国女药学家屠呦呦因创新性抗疟药青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖.颁奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.下列关于青蒿素和双氢青蒿素(结构如图)说法错误的是( )| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 由青蒿素制备双氢青蒿素的反应属还原反应 | |
| C. | 青蒿素和双氢青蒿素均能跟氢氧化钠反应 | |
| D. | 青蒿素分子中含有过氧键和酯基、醚键 |
17.2010年诺贝尔化学奖授予在“钯催化交叉偶联反应”领域作出突出贡献的三位化学家.下列有关钯原子(${\;}_{46}^{106}$Pd)的说法不正确的是( )
| A. | 质量数为106 | B. | 质子数为46 | C. | 电子数为46 | D. | 中子数为46 |
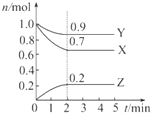 某温度时,在2L 容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.
某温度时,在2L 容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.