题目内容
16.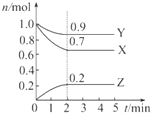 某温度时,在2L 容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.
某温度时,在2L 容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示. (1)由图中数据分析,该反应的化学方程式为:3X+Y?2Z.
(2)反应开始至2min,Z的平均反应速率为0.05mol•L-1•min-1.
(3)判断:第2min时,反应是否达到平衡?是,第2min 时,Z的生成速率与Z的消耗速率相比相等(填“大”、“小”或“相等”).
分析 (1)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;
(2)分析图象计算Z的消耗物质的量为0.2mol,结合反应速率概念计算,V=$\frac{△c}{△t}$;
(3)反应物和生成物物质的量不再变化说明反应达到平衡状态,此时正逆反应速率相同.
解答 解:(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则反应的化学方程式为:3X+Y?2Z,
故答案为:3X+Y?2Z;
(2)图象计算Z的消耗物质的量为0.2mol,从开始至2min,Z的平均反应速率=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L•min);
故答案为:0.05mol/(L•min);
(3)图象分析可知第2min时,XYZ的物质的量不随时间的变化而变化,说明反应达到平衡状态,Z的生成速率与Z的消耗速率相等,
故答案为:是;相等.
点评 本题考查了化学反应速率、化学平衡状态判断,主要是概念的计算应用,掌握基础是解题关键,题目较简单.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
6.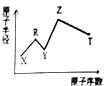 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离子平衡.六种元素的原子半径与原序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离子平衡.六种元素的原子半径与原序数的关系如图所示.下列推断正确的是( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离子平衡.六种元素的原子半径与原序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离子平衡.六种元素的原子半径与原序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 与同主族元素的氢化物相比较,R和Y的氢化物最稳定 | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 由X、Y、Z、T四种元素组成的化合物水溶液一定显碱性 |
7.氧化铜矿用稀硫酸溶解后所得酸浸液(含Cu2+、H+、SO42-、Mg2+、A13+、Fe2+) 经下列流程可制得高纯度硫酸铜晶体如图1:
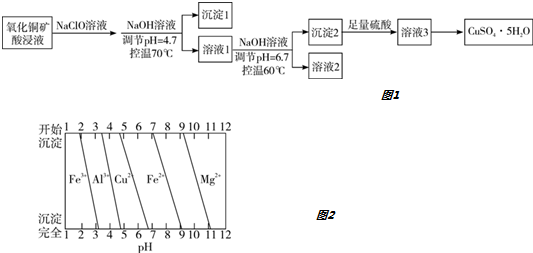
已知:该实验条件下,各金属离子沉淀的pH如图2所示.下列判断正确的是( )

已知:该实验条件下,各金属离子沉淀的pH如图2所示.下列判断正确的是( )
| A. | 沉淀1的主要成分为Al(OH)3和Fe(OH)3 | |
| B. | 溶液2中所含金属阳离子只有Mg2+ | |
| C. | 将溶液3蒸干即得CuSO4•5H2O晶体 | |
| D. | 若不加入NaClO溶液,对制得硫酸铜晶体的纯度将无影响 |
4.汽车尾气是造成雾霾天气的重要原因之一,尾气中的主要污染物为CxHy、NO、CO、SO2及固体颗粒物等.研究汽车尾气的成分及其发生的反应,可以为更好的治理汽车尾气提供技术支持.请回答下列问题:
(1)治理尾气中NO和CO的一种方法是:在汽车排气管上装一个催化转化装置,使二者发生反应转化成无毒无污染气体,该反应的化学方程式是2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
(2)活性炭也可用于处理汽车尾气中的NO.在1L恒容密闭容器中加入0.1000molNO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量以及容器内压强如下表:
根据上表数据,写出容器中发生反应的化学方程式C+2NO?N2+CO2并判断p>3.93MPa(用“>”、“<“或“=”填空).计算反应体系在200℃时的平衡常数Kp=0.5625(用平衡分压代替平衡浓度计算,分压=总压×体积分数).
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液.常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Kal(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)=4.2×10-9.
(4)尾气中的碳氢化合物含有甲烷,其在排气管的催化转化器中可发生如下反应CH4(g)+H2O(1)?CO(g)+3H2 (g)△H=+250.1kJ.mol-l.已知CO(g)、H2(g)的燃烧热依次为283.0kJ.mol-1、285.8kJ.mol-1,请写出表示甲烷燃烧热的热化学方程式CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=-890.3KJ/mol.以CH4(g)为燃料可以设计甲烷燃料电池,该电 池以稀H2SO4作电解质溶液,其负极电极反应式为CH4-8e-+2H2O=CO2+8H+,已知该电池的能量转换效率为86.4%,则该电池的比能量为13.3kW.h.kg-1(结果保留1位小数,比能量=$\frac{电池输出电能(kW•h)}{燃料质量(kg)}$,lkW•h=3.6×1 06J).
(1)治理尾气中NO和CO的一种方法是:在汽车排气管上装一个催化转化装置,使二者发生反应转化成无毒无污染气体,该反应的化学方程式是2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
(2)活性炭也可用于处理汽车尾气中的NO.在1L恒容密闭容器中加入0.1000molNO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量以及容器内压强如下表:
| 活性炭/mol | NO/mol | A/mol | B/mol | P/MPa | |
| 200℃ | 2.000 | 0.0400 | 0.0300 | 0.0300 | 3.93 |
| 335℃ | 2.005 | 0.0500 | 0.0250 | 0.250 | P |
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液.常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Kal(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)=4.2×10-9.
(4)尾气中的碳氢化合物含有甲烷,其在排气管的催化转化器中可发生如下反应CH4(g)+H2O(1)?CO(g)+3H2 (g)△H=+250.1kJ.mol-l.已知CO(g)、H2(g)的燃烧热依次为283.0kJ.mol-1、285.8kJ.mol-1,请写出表示甲烷燃烧热的热化学方程式CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=-890.3KJ/mol.以CH4(g)为燃料可以设计甲烷燃料电池,该电 池以稀H2SO4作电解质溶液,其负极电极反应式为CH4-8e-+2H2O=CO2+8H+,已知该电池的能量转换效率为86.4%,则该电池的比能量为13.3kW.h.kg-1(结果保留1位小数,比能量=$\frac{电池输出电能(kW•h)}{燃料质量(kg)}$,lkW•h=3.6×1 06J).
1.为防止NO2污染空气,科学家寻求合适的化合物G和催化剂,以实现反应:NO2+G $\stackrel{催化剂}{?}$N2+H2O+nZ (未配平,n可以为0),上述反应式中的G不可能是( )
| A. | CO | B. | NH3 | C. | H2O2 | D. | CH3CH2OH |
8.下列实验目的对应的实验操作和实验原理均正确的是( )
| 实验目的 | 实验操作 | 实验原理 | |
| A | 提纯混有少量硝酸钾的氯化钠 | 在较高温度下制得浓溶液再冷却结晶、过滤、干燥 | 氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升高显著增大 |
| B | 配制FeCl3溶液 | 将FeCl3固体溶解于适量硫酸溶液 | H+抑制FeCl3水解 |
| C | 检验溶液中是否含有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | NH3溶于水后溶质的主要存在形式是NH4+、OH- |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡 | 3Mg(OH)2+2Fe3+?2Fe(OH)3+3Mg2+ |
| A. | A | B. | B | C. | C | D. | D |
5.饱和二氧化硫水溶液中存在下列平衡体系:
SO2+H2O?H++HS${O}_{3}^{-}$
HS${O}_{3}^{-}$?H++S${O}_{3}^{2-}$
若向此溶液中( )
SO2+H2O?H++HS${O}_{3}^{-}$
HS${O}_{3}^{-}$?H++S${O}_{3}^{2-}$
若向此溶液中( )
| A. | 加水,S${O}_{3}^{2-}$浓度增大 | |
| B. | 通入少量Cl2气体,溶液pH增大 | |
| C. | 加少量CaSO3粉末,HS${O}_{3}^{-}$ 浓度基本不变 | |
| D. | 通入少量HCl气体,溶液中HS${O}_{3}^{-}$ 浓度减小 |
12.能说明Cl的非金属性比S的非金属性强的事实是( )
| A. | H2S的水溶液中滴加新制氯水后出现浑浊 | |
| B. | Cl原子最外层有7个电子,而S原子最外层有6个电子 | |
| C. | HCl水溶液的酸性强于H2S水溶液的酸性 | |
| D. | HClO4的酸性比H2SO3的酸性强 |