题目内容
下列说法正确的是( )
| A、被氧化的物质是氧化剂 |
| B、可以利用酒精将碘水中的碘提取出来 |
| C、化合反应一定不是氧化还原反应 |
| D、铝抗腐蚀是外层氧化膜致密的缘故 |
考点:氧化还原反应,金属的电化学腐蚀与防护
专题:氧化还原反应专题
分析:A.被氧化的物质应为还原剂;
B.酒精和水混溶,不能用作萃取剂;
C.化合反应如存在化合价的变化,为氧化还原反应;
D.致密的氧化物膜可阻碍反应的进行.
B.酒精和水混溶,不能用作萃取剂;
C.化合反应如存在化合价的变化,为氧化还原反应;
D.致密的氧化物膜可阻碍反应的进行.
解答:
解:A.氧化还原反应中,被氧化的物质应为还原剂,故A错误;
B.酒精和水混溶,不能用作萃取剂,萃取剂与水互不相溶,故B错误;
C.化合反应如存在化合价的变化,为氧化还原反应,如H2+Cl2=2HCl,故C错误;
D.铝被氧化可生成致密的氧化物膜,可阻碍反应的进行,故D正确.
故选D.
B.酒精和水混溶,不能用作萃取剂,萃取剂与水互不相溶,故B错误;
C.化合反应如存在化合价的变化,为氧化还原反应,如H2+Cl2=2HCl,故C错误;
D.铝被氧化可生成致密的氧化物膜,可阻碍反应的进行,故D正确.
故选D.
点评:本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意把握物质的性质,从元素化合价的角度解答,难度不大.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )
| A、硝酸钠 氢氧化钠 |
| B、氧化铜 二氧化锰 |
| C、氯化钾 碳酸钙 |
| D、硫酸铜 氢氧化钠 |
24mL浓度为0.05mol/L的Na2SO3溶液恰好与20mL某浓度的K2Cr2O7溶液完全反应.已知Na2SO3被K2Cr2O7氧化为Na2SO4,且元素Cr在还原产物中的化合价为+3价,则原K2Cr2O7溶液的物质的量浓度为( )
| A、0.01mol/L |
| B、0.02mol/L |
| C、0.03mol/L |
| D、0.04mol/L |
下列可逆反应达到平衡后,增大压强同时降低温度,平衡一定向右移动的是( )
| A、2AB(g)?A2(g)+B2(g)△H>0 |
| B、A2(g)+3B2(g)?2AB3(g)△H<0 |
| C、A(s)+B(g)?C(g)+D(g)△H>0 |
| D、2A(g)+B(g)?3C(g)+D(s)△H<0 |
将100ml 2mol/lAlCl3溶液跟一定体积的4mol/lNaOH溶液混合后可得7.8g沉淀.则NaOH溶液的体积可能是( )
| A、90ml | B、150ml |
| C、175ml | D、200ml |
已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )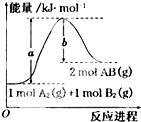

| A、每生成2分子AB吸收bkJ热量 |
| B、加入催化剂,该化学反应的反应热变大 |
| C、断裂1molA-A和1molB-B键,放出akJ能量 |
| D、该反应热△H=+(a-b)kJ/mol |