题目内容
通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )
| A、硝酸钠 氢氧化钠 |
| B、氧化铜 二氧化锰 |
| C、氯化钾 碳酸钙 |
| D、硫酸铜 氢氧化钠 |
考点:物质的分离、提纯和除杂
专题:化学实验基本操作
分析:能够通过用水溶解、过滤、蒸发等操作分离的物质要具有以下特点:一种物质溶于水,一种物质不溶于水,两种物质都溶于水或都不溶于水是不能分离的.
解答:
解:A.硝酸钠、氢氧化钠都溶于水,不能分离,故A错误;
B.氧化铜、二氧化锰都不溶于水,也不能分离,故B错误;
C.碳酸钙不溶于水,氯化钾溶于水,所以先加水溶解再进行过滤,即可分离,故C正确;
D.硫酸铜不溶于水,且两者反应生成氢氧化铜和硫酸钠,也不能分离,故D错误.
故选C.
B.氧化铜、二氧化锰都不溶于水,也不能分离,故B错误;
C.碳酸钙不溶于水,氯化钾溶于水,所以先加水溶解再进行过滤,即可分离,故C正确;
D.硫酸铜不溶于水,且两者反应生成氢氧化铜和硫酸钠,也不能分离,故D错误.
故选C.
点评:本题考查混合物的分离,难度不大,明确一种物质溶于水,一种物质不溶于水的分离方法是先用水溶解、再过滤、最后蒸发即可解答.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
PCl3和PCl5都是重要的化工原料.将PCl3(g) 和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,并于10 min时达到平衡:PCl3(g)+Cl3(g)?PCl3(g).有关数据如下:
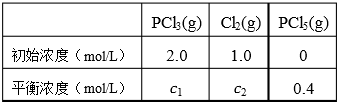
下列判断不正确的是( )

下列判断不正确的是( )
| A、10 min内,v(Cl2)=0.04 mol/(L?min) |
| B、当容器中Cl2为1.2 mol时,反应达到平衡 |
| C、升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的转化率变大 |
| D、平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
某种兴奋剂是奥运会上最早使用并最早被禁用,其结构简式如下:下列有关叙述正确的是( )
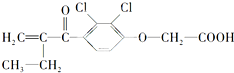

| A、该物质属于芳香族化合物,分子式为C13H12O4Cl2 |
| B、该物质分子内处于同一平面的碳原子不超过7个 |
| C、1 mol该物质最多可与5 mol H2发生加成反应 |
| D、1 mol该物质最多可与含3 mol NaOH的水溶液发生反应 |
在一定条件下,可逆反应:A(g)+3B(g)?4C(g)达到平衡时,下列叙述正确的是( )
| A、此时反应物B全部转化成了生成物 |
| B、单位时间内生成n mol A,同时生成4n mol C |
| C、若改变条件,A、B、C的浓度不可能再变化 |
| D、A、B、C的分子数比为1:3:4 |
下列说法正确的是( )
| A、被氧化的物质是氧化剂 |
| B、可以利用酒精将碘水中的碘提取出来 |
| C、化合反应一定不是氧化还原反应 |
| D、铝抗腐蚀是外层氧化膜致密的缘故 |
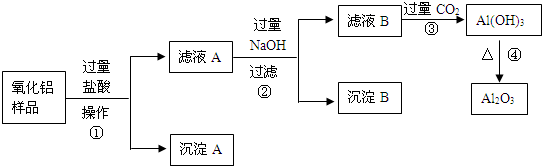
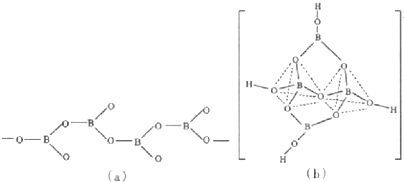
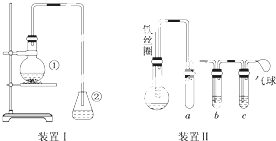 为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验: