题目内容
(1)含铬化合物有毒,对人畜危害很大.因此含铬废水必须进行处理才能排放.
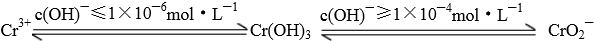
已知:
在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去.
①写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式 .
②完成用离子方程式表示溶液pH不能超过10(即c(OH)-≥1×10-4mol?L-1)的原因为Cr(OH)3+OH-= +2H2O.
(2)在硝酸工业生产吸收塔中,将硝酸生产中排出的尾气(体积分数:含0.5% NO、1.5% NO2)用纯碱溶液完全吸收,完成反应方程式:NO+3NO2+2Na2CO3=3NaNO2+NaNO3+2 ,该反应中能用纯碱代替氢氧化钠溶液发生反应的原因是利用了Na2CO3水解呈现的 性.
(3)一定浓度的HF和Al2(SO4)3混合液中,铝的各种微粒含量?随pH的分布曲线如图示.用NaOH使混合液的pH从5调整到7,完成有关反应的离子方程式为:
+3OH-=Al(OH)3↓+2F-;
+3OH-=Al(OH)3↓+3F-.
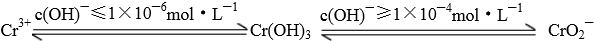
已知:

在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去.
①写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式
②完成用离子方程式表示溶液pH不能超过10(即c(OH)-≥1×10-4mol?L-1)的原因为Cr(OH)3+OH-=
(2)在硝酸工业生产吸收塔中,将硝酸生产中排出的尾气(体积分数:含0.5% NO、1.5% NO2)用纯碱溶液完全吸收,完成反应方程式:NO+3NO2+2Na2CO3=3NaNO2+NaNO3+2
(3)一定浓度的HF和Al2(SO4)3混合液中,铝的各种微粒含量?随pH的分布曲线如图示.用NaOH使混合液的pH从5调整到7,完成有关反应的离子方程式为:
考点:离子方程式的有关计算,氧化还原反应的计算
专题:计算题
分析:(1)①二价铁离子有还原性,Cr2O72-有强氧化性,二者能发生氧化还原反应,根据电子得失配平;
②由题意可知,当pH超过10即c(OH-)≥10-4mol?L-1时,Cr(OH)3转变成CrO2-;
(2)根据原子守恒来确定物质的化学式;强碱弱酸盐水解显示碱性;
(3)由图可知溶液pH=5时,混合液中铝的微粒为AlF2+、AlF3,pH值=7时,铝的微粒为Al(OH)3,即AlF2+、AlF3与OH-反应生成Al(OH)3、F-.
②由题意可知,当pH超过10即c(OH-)≥10-4mol?L-1时,Cr(OH)3转变成CrO2-;
(2)根据原子守恒来确定物质的化学式;强碱弱酸盐水解显示碱性;
(3)由图可知溶液pH=5时,混合液中铝的微粒为AlF2+、AlF3,pH值=7时,铝的微粒为Al(OH)3,即AlF2+、AlF3与OH-反应生成Al(OH)3、F-.
解答:
解:(1)二价铁离子有还原性,Cr2O72-有强氧化性,二者能发生氧化还原反应,二价铁离子被氧化成三价铁离子,Cr2O72-被还原为Cr3+,反应方程式为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,故答案为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O;
②由题意可知,当pH超过10即c(OH-)≥10-4mol?L-1时,Cr(OH)3转变成CrO2-,发生Cr(OH)3+OH-═CrO2-+2H2O,故答案为:CrO2-;
(2)根据原子守恒,则缺少物质的化学式为:CO2,碳酸钠是强碱弱酸盐,水解显示碱性,故答案为:CO2;碱;
(3)由图可知溶液pH=5时,混合液中铝的微粒为AlF2+、AlF3,pH值=7时,铝的微粒为Al(OH)3,即AlF2+、AlF3与OH-反应生成Al(OH)3、F-,反应离子方程式为:AlF2++3OH-=Al(OH)3↓+2F-、AlF3+3OH-=Al(OH)3↓+3F-,故答案为:AlF2+;AlF3.
②由题意可知,当pH超过10即c(OH-)≥10-4mol?L-1时,Cr(OH)3转变成CrO2-,发生Cr(OH)3+OH-═CrO2-+2H2O,故答案为:CrO2-;
(2)根据原子守恒,则缺少物质的化学式为:CO2,碳酸钠是强碱弱酸盐,水解显示碱性,故答案为:CO2;碱;
(3)由图可知溶液pH=5时,混合液中铝的微粒为AlF2+、AlF3,pH值=7时,铝的微粒为Al(OH)3,即AlF2+、AlF3与OH-反应生成Al(OH)3、F-,反应离子方程式为:AlF2++3OH-=Al(OH)3↓+2F-、AlF3+3OH-=Al(OH)3↓+3F-,故答案为:AlF2+;AlF3.
点评:本题考查了氧化还原反应离子方程式的书写、电极反应式的书写,注意氧化还原反应中利用得失电子守候配平方程,难度中等.

练习册系列答案
相关题目
将两支惰性电极插入CuSO4溶液中,通电电解,当有1×10-3mol的OH-放电时,溶液显浅蓝色,则下列叙述正确的是( )
| A、阳极上析出5.6mL O2(标准状况) |
| B、阴极上析出64mg Cu |
| C、阴极上析出11.2mL H2(标准状况) |
| D、阳极和阴极质量都无变化 |
在水中加入等物质的量的Ag+、Ba2+、SO42-、NO3-、Cl-、Na+,用惰性材料作电极进行电解,通电片刻后停止,下列说法不正确的是( )
| A、电解的实质是:阳极:2Cl--2e-=Cl2↑;阴极:Ag+e-=Ag |
| B、电解的实质是:阳极:4OH--4e-=2H2O+O2↑;阴极:2H++2e-=H2↑ |
| C、要恢复成电解前的溶液可以加水 |
| D、电解产物中氧化产物和还原产物的物质的量之比为1:2 |
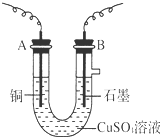 某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)
某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)