题目内容
将过量CO2通入NaOH和Ca(OH)2的混合稀溶液中,生成沉淀的质量(m)和通入CO2(V)关系图,正确的是( )
A、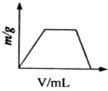 |
B、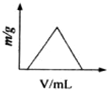 |
C、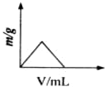 |
D、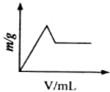 |
考点:离子方程式的有关计算
专题:图示题
分析:NOH和Ca(OH)2的混合稀溶液中通入CO2,发生反应:2OH-+CO2=CO32-+H2O,Ca2++CO32-=CaCO3↓,当氢氧化钙消耗完时,继续通入二氧化碳,二氧化碳和碳酸钠反应生成碳酸氢钠,反应的离子方程式为:CO32-+H2O+CO2=2HCO3-,继续通入二氧化碳,二氧化碳和碳酸钙、水反应生成可溶性的碳酸氢钙,反应的离子方程式为:
CaCO3+C2O+CO2=Ca2++2HCO3-,据此分析图象.
CaCO3+C2O+CO2=Ca2++2HCO3-,据此分析图象.
解答:
解:NOH和Ca(OH)2的混合稀溶液中通入CO2,开始二氧化碳与氢氧化钙反应生成碳酸钙,此时沉淀质量增加,发生反应:2OH-+CO2=CO32-+H2O,Ca2++CO32-=CaCO3↓,当氢氧化钙消耗完时,继续通入二氧化碳,二氧化碳和碳酸钠反应生成碳酸氢钠,但是同时沉淀的质量也不会减少,反应的离子方程式为:
CO32-+H2O+CO2=2HCO3-,继续通入二氧化碳,二氧化碳和碳酸钙、水反应生成可溶性的碳酸氢钙,此时沉淀逐渐减少最后为零,反应的离子方程式为:CaCO3+C2O+CO2=Ca2++2HCO3-,分析所给的选项可以知道选项A符合刚才的分析,即A是正确的.
故选A.
CO32-+H2O+CO2=2HCO3-,继续通入二氧化碳,二氧化碳和碳酸钙、水反应生成可溶性的碳酸氢钙,此时沉淀逐渐减少最后为零,反应的离子方程式为:CaCO3+C2O+CO2=Ca2++2HCO3-,分析所给的选项可以知道选项A符合刚才的分析,即A是正确的.
故选A.
点评:本考点主要考查了二氧化碳的化学性质,二氧化碳能使石灰水变浑浊,这是二氧化碳的特性,特别是性质与图象结合的题型,一定要认真分析,综合把握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
两个完全相同的烧杯中分别加入同体积同浓度的2mol/L的硫酸,放置于天平的两端,天平平衡,分别加入10.8克的Al和Mg,待反应完毕后,天平的平衡情况( )
| A、一定是加入金属镁的一端下倾 |
| B、一定是加入金属铝的一端下倾 |
| C、一定是仍然保持平衡 |
| D、无法判断 |
下列说法错误的是( )
| A、回收照相业中的定影液可提取镁 |
| B、回收不锈钢可提取铬或镍以及铁 |
| C、回收可口可乐易拉罐可回收铝 |
| D、回收精炼铜的阳极泥可得金、银等贵金属 |
为了测定铜铁合金中铜的质量分数,在10.00g试样中加入200mL、0.6mol/L的稀硝酸,充分反应后剩余金属7.48g,再向其中加入50mL、0.4mol/L的稀硫酸,充分振荡后剩余金属6.60g.若硝酸的还原产物只有NO,下列说法正确的是( )
| A、上述测定不能达到实验目的 |
| B、剩余的7.48g金属为铜 |
| C、共生成NO气体0.04mol |
| D、该合金中铜的质量分数为69.2% |

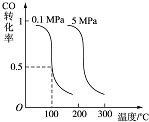 CO可用于合成甲醇.在压强为0.1MPa条件下,在体积为bL的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:CO(g)+2H2(g)?CH3OH(g)平衡时CO的转化率与温度、压强的关系如图:
CO可用于合成甲醇.在压强为0.1MPa条件下,在体积为bL的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:CO(g)+2H2(g)?CH3OH(g)平衡时CO的转化率与温度、压强的关系如图: