题目内容
9.从1L H2SO4溶液A中取出100mL,然后将此100mL溶液稀释得到400mL 0.01mol•L-1 H2SO4溶液B,则H2SO4溶液A的物质的量浓度为( )| A. | 0.01mol•L-1 | B. | 0.04mol•L-1 | C. | 0.08mol•L-1 | D. | 0.16mol•L-1 |
分析 抓住稀释前后溶质的物质的量不变,所以100mL溶液中硫酸的物质的量为:0.4L×0.01mol•L-1 =0.004mol,根据c=$\frac{n}{V}$,进行计算求解.
解答 解:100mL溶液中硫酸的物质的量为:0.4L×0.01mol•L-1 =0.004mol,所以1L H2SO4溶液中溶质A的物质的量为:0.004mol×$\frac{1000}{100}$=0.04mol,则c=$\frac{n}{V}$=$\frac{0.04mol}{1L}$=0.04mol•L-1,故选B.
点评 本题考查溶液的稀释问题,学生要抓住稀释过程中溶质的物质的量不变,然后结合公式c=$\frac{n}{V}$进行解题,比较容易.

练习册系列答案
相关题目
19.室温下,取浓度都为0.05mol•L-1的NaOH和HCl溶液,以一定的体积比相混合,所得溶液的pH等于12,则两溶液的体积比为( )
| A. | 4:3 | B. | 3:4 | C. | 3:2 | D. | 2:3 |
20.下列生活中常见的变化中,均属于化学变化的一组是( )
| A. | 工业制氧、钢铁生锈 | B. | 石蜡熔化、干冰升华 | ||
| C. | 粮食酿酒、烟花燃放 | D. | 汽油挥发、云消雾散 |
17.含气体杂质的乙炔4.16g与H2加成生成饱和链烃,共用去4.48L(标准状况)H2,则气体杂质不可能是( )
| A. | 乙烯 | B. | 丙炔 | C. | 丁二烯 | D. | 甲烷 |
4.电解100ml含c(H+)=0.40mol/L的下列溶液.当电路中通过0.04mol电子时,理论上析出金属质量最大的是( )
| A. | 0.10mol/L Ag+ | B. | 0.20mol/L Zn2+ | C. | 0.20mol/L Cu2+ | D. | 0.20mol/L Pb2+ |
14.电泳时,硫化砷胶粒移向正极.要使一定量硫化砷溶液聚沉下列盐中需用的物质的量最小的是( )
| A. | NaCl | B. | CaCl2 | C. | AlCl3 | D. | MgSO4 |
4.下列物质的系统命名中,错误的是( )
| A. | 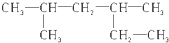 2,4-二甲基己烷 2,4-二甲基己烷 | |
| B. | 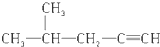 2-甲基-4-戊炔 2-甲基-4-戊炔 | |
| C. | 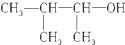 3-甲基-2-丁醇 3-甲基-2-丁醇 | |
| D. | CH3-CHBr-CHBr-CH3 2,3-二溴丁烷 |
 .
.