题目内容
14.电泳时,硫化砷胶粒移向正极.要使一定量硫化砷溶液聚沉下列盐中需用的物质的量最小的是( )| A. | NaCl | B. | CaCl2 | C. | AlCl3 | D. | MgSO4 |
分析 电泳时,硫化砷胶粒移向正极,说明硫化砷胶粒吸附负电荷,要使一定量硫化砷溶液聚沉加入电解质溶液中阳离子所带电荷数越多,胶体聚沉越快,需要的物质的量越小.
解答 解:电泳时,硫化砷胶粒移向正极,说明硫化砷胶粒吸附负电荷,要使一定量硫化砷溶液聚沉加入电解质溶液中阳离子所带电荷数越多,胶体聚沉越快,需要的物质的量越小选项中氯化铝溶液中铝离子所带电荷数最多.,要使一定量硫化砷溶液聚沉需用的物质的量最小,故选C.
点评 本题考查了胶体性质、胶体电泳的性质分析判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
5.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | 1.0 mol•L-1的KNO3溶液中:Fe2+、H+、Cl-、I- | |
| B. | 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN- | |
| C. | 常温下,在c(H+)/c(OH-)=1×1012的溶液:NH4+、Mg2+、C1-、K+ | |
| D. | 水电离的c(H+)=1×10-13 mol•L-1的溶液中:K+、Na+、AlO2-、CO32- |
2.容量瓶上需标有以下5项中的哪些内容?①温度 ②浓度 ③容量 ④压强 ⑤刻度线( )
| A. | ①③⑤ | B. | ③④⑤ | C. | ①②④ | D. | ②③④ |
9.从1L H2SO4溶液A中取出100mL,然后将此100mL溶液稀释得到400mL 0.01mol•L-1 H2SO4溶液B,则H2SO4溶液A的物质的量浓度为( )
| A. | 0.01mol•L-1 | B. | 0.04mol•L-1 | C. | 0.08mol•L-1 | D. | 0.16mol•L-1 |
11.如表列出了①~⑩十种元素在周期表中前四周期的位置,请回答下列问题:(填元素符号或化学式)
(1)在这十种元素形成的单质中化学性质最不活泼的是Ar;金属性最强的是K;非金属性最强的是E;能导电的单质有5种.
(2)①、③两元素的氧化物对应的水化物中碱性强的是NaOH;(填化学式,下同.)⑤、⑦两元素的最高价氧化物对应的水化物中酸性强的是H2SO4,用一个化学方程式证明Na2CO3+H2SO4=CO2↑+Na2SO4+H2O.
(3)①、②、③三元素按原子半径由小到大的顺序排列为Mg<Na<K.
(4)写出由②、⑨两元素组成物质的电子式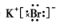 .
.
(5)①的氧化物对应的水化物与④的氯化物反应的离子方程式,因物质的量配比不同产物有所不同,试分别写出有关反应的离子方程式Al3++3OH-=Al(OH)3↓、Al3++4OH-=AlO2-+2H2O.
| 主族族数 周期序数 | ||||||||
| ⑤ | ⑥ | ⑧ | ||||||
| ① | ③ | ④ | ⑦ | ⑩ | ||||
| ② | ⑨ |
(2)①、③两元素的氧化物对应的水化物中碱性强的是NaOH;(填化学式,下同.)⑤、⑦两元素的最高价氧化物对应的水化物中酸性强的是H2SO4,用一个化学方程式证明Na2CO3+H2SO4=CO2↑+Na2SO4+H2O.
(3)①、②、③三元素按原子半径由小到大的顺序排列为Mg<Na<K.
(4)写出由②、⑨两元素组成物质的电子式
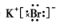 .
.(5)①的氧化物对应的水化物与④的氯化物反应的离子方程式,因物质的量配比不同产物有所不同,试分别写出有关反应的离子方程式Al3++3OH-=Al(OH)3↓、Al3++4OH-=AlO2-+2H2O.
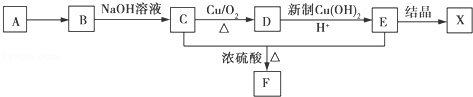
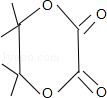 .
. ,可以证明该结论的实验是(用离子方程式表示)Cl2+S2-=2Cl-+S↓.
,可以证明该结论的实验是(用离子方程式表示)Cl2+S2-=2Cl-+S↓.