题目内容
给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
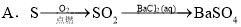
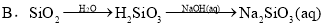
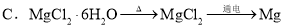

练习册系列答案
相关题目
14.运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义.
(1)已知反应CO(g)+2H2(g)?CH3OH(g)△H=-99kJ•mol-1中的相关化学键能如表:
则x=1076.
(2)甲醇作为一种重要的化工原料,既可以作为燃料,还可用于合成其它化工原料.在一定条件下可利用甲醇羰基化法制取甲酸甲酯,其反应原理可表示为:CH3OH(g)+CO(g)?HCOOCH3(g)△H=-29.1kJ•mol-1.向体积为2L的密闭容器中充入2mol CH3OH(g) 和2mol CO,测得容器内的压强(p:kPa)随时间(min)的变化关系如图1中Ⅰ、Ⅱ、Ⅲ曲线所示:

①Ⅱ和Ⅰ相比,改变的反应条件是使用催化剂.
②反应Ⅰ在5min时达到平衡,在此条件下从反应开始到达到平衡时v(HCOOCH3)=0.10mol•L-1•min-1.
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=2L•mol-1.在体积和温度不变的条件下,在上述反应达到平衡Ⅱ时,再往容器中加入1mol CO和2mol HCOOCH3后v(正)< v(逆) (填“>”“<”“﹦”),原因是浓度商Qc=$\frac{1.5}{0.5•1}$=3>2=K反应向逆方向进行,故v(正)<v(逆).
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1>T3(填“>”“<”“﹦”),判断的理由是此反应为放热反应,降温,平衡向正向进行(或反应Ⅰ达平衡时所需的时间比反应Ⅲ达平衡时所需的时间短,反应速率快,故T1温度更高).
(3)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2.某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,测得NO转化为N2的转化率随温度、CO混存量的变化情况如图2所示,利用以下反应填空:
NO+CO?N2+CO2(有CO) 2NO?N2+O2(无CO)
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为此反应为放热反应,升高温度反应更有利于向逆反应方向进行.
②在$\frac{n(NO)}{n(CO)}$=1的条件下,应控制最佳温度在870℃左右.
(1)已知反应CO(g)+2H2(g)?CH3OH(g)△H=-99kJ•mol-1中的相关化学键能如表:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | x | 465 | 413 |
(2)甲醇作为一种重要的化工原料,既可以作为燃料,还可用于合成其它化工原料.在一定条件下可利用甲醇羰基化法制取甲酸甲酯,其反应原理可表示为:CH3OH(g)+CO(g)?HCOOCH3(g)△H=-29.1kJ•mol-1.向体积为2L的密闭容器中充入2mol CH3OH(g) 和2mol CO,测得容器内的压强(p:kPa)随时间(min)的变化关系如图1中Ⅰ、Ⅱ、Ⅲ曲线所示:

①Ⅱ和Ⅰ相比,改变的反应条件是使用催化剂.
②反应Ⅰ在5min时达到平衡,在此条件下从反应开始到达到平衡时v(HCOOCH3)=0.10mol•L-1•min-1.
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=2L•mol-1.在体积和温度不变的条件下,在上述反应达到平衡Ⅱ时,再往容器中加入1mol CO和2mol HCOOCH3后v(正)< v(逆) (填“>”“<”“﹦”),原因是浓度商Qc=$\frac{1.5}{0.5•1}$=3>2=K反应向逆方向进行,故v(正)<v(逆).
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1>T3(填“>”“<”“﹦”),判断的理由是此反应为放热反应,降温,平衡向正向进行(或反应Ⅰ达平衡时所需的时间比反应Ⅲ达平衡时所需的时间短,反应速率快,故T1温度更高).
(3)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2.某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,测得NO转化为N2的转化率随温度、CO混存量的变化情况如图2所示,利用以下反应填空:
NO+CO?N2+CO2(有CO) 2NO?N2+O2(无CO)
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为此反应为放热反应,升高温度反应更有利于向逆反应方向进行.
②在$\frac{n(NO)}{n(CO)}$=1的条件下,应控制最佳温度在870℃左右.
15.下列溶液中Na+与50mL 3mol•L-1 NaCl溶液中Na+物质的量浓度相等的是( )
| A. | 150 mL 1 mol•L-1Na3PO4溶液 | B. | 75 mL 2 mol•L-1NaNO3溶液 | ||
| C. | 75 mL 3 mol•L-1Na2SO4溶液 | D. | 150 mL 2mol•L-1NaCl溶液 |


 溶液加入到120mL盐酸中,所得溶液的pH为2。如果混合前氢氧化钠溶液和盐酸的物质的量浓度相同,它们的浓度是 ( )
溶液加入到120mL盐酸中,所得溶液的pH为2。如果混合前氢氧化钠溶液和盐酸的物质的量浓度相同,它们的浓度是 ( )

 ≈4.0]。
≈4.0]。
 NO
NO 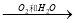 HNO3
HNO3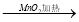 Cl2
Cl2  漂白粉
漂白粉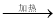 无水MgCl2
无水MgCl2  Mg
Mg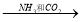 NaHCO3
NaHCO3 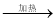 Na2CO3
Na2CO3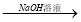 NaAlO2溶液
NaAlO2溶液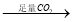 Al(OH)3
Al(OH)3 Al2O3
Al2O3  Al
Al