题目内容
17.某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如下图所示(夹持仪器已略去).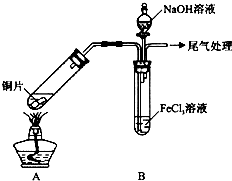
(1)实验前,应先检查装置的气密性;实验中产生的尾气应通人NaOH溶液.
(2)实验过程中需要配制100mL1mol/L FeCl3溶液(未用浓盐酸酸化),所需要的玻璃仪器有:烧杯、量筒、玻璃棒、100mL容量瓶、胶头滴管.
(3)该小组同学向5mL lmol/L FeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是开始无现象,然后产生白色沉淀.
(4)该小组同学在(3)中实验时,发现溶液变为浅绿色需要较长时间,在此期间同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象,最终溶液呈浅绿色.
【查阅资料】Fe(HSO3)2+离子在溶液中呈红棕色且具有较强的还原性,能被Fe3+氧化为SO42-.
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是Fe3++H2O+Fe(HSO3)2+═2Fe2++SO42-+3H+.
(5)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了如下实验:
| 步骤② | 往5mL1mol•L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色.微热3min,溶液颜色变为浅绿色. |
| 步骤③ | 往5mL重新配制的1mol•L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色.几分钟后,发现溶液颜色变成浅绿色. |
(6)综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程.
分析 向FeCl3溶液中通人足量的SO2,再加入NaOH溶液,需先中溶液中的H+,在沉淀Fe2+,现象为开始没有明显现象,后有白色沉淀生成;结合电荷守恒和质量守恒,可以确定离子方程式:Fe3++H2O+Fe(HSO3)2+=2Fe2++SO42-+3H+;(5)均会发生反应生成Fe2+,加入K3[Fe(CN)6]生成蓝色的铁氰化亚铁;通过实验得出结论:加热或提高FeCl3溶液的酸性会缩短浅绿色出现的时间,
(1)制取气体的反应装置,制取之前应检查装置的气密性;二氧化硫尾气用NaOH溶液吸收;
(2)据配制一定物质的量浓度的溶液需要的仪器分析;
(3)FeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,为FeCl2溶液,溶液显酸性;
(4)Fe(HSO3)2+离子可以将Fe3+还原为Fe2+,根据氧化还原反应特征书写离子方程式;
(5)铁氰化钾溶液与二价铁离子反应生成蓝色的Fe3(Fe(CN)6)2;
(6)综合上述实验分析,升高温度、提高FeCl3溶液的酸性会加快反应速率,缩短浅绿色出现的时间.
解答 解:(1)制取气体的反应装置,制取之前应检查装置的气密性;二氧化硫尾气用NaOH溶液吸收,
故答案为:气密性;NaOH;
(2)配制100mL1mol/L FeCl3溶液,所需要的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管、100mL的容量瓶,
故答案为:胶头滴管、100mL的容量瓶;
(3)溶液显酸性,滴入NaOH溶液时,开始无现象,然后产生白色沉淀,
故答案为:开始无现象,然后产生白色沉淀;
(4)Fe(HSO3)2+离子可以将Fe3+还原为Fe2+,则由氧化还原反应有升必有降,则离子方程式为:Fe3++H2O+Fe(HSO3)2+═2Fe2++SO42-+3H+;
故答案为:Fe3++H2O+Fe(HSO3)2+═2Fe2++SO42-+3H+;
(5)铁氰化钾溶液与二价铁离子反应生成蓝色的Fe3(Fe(CN)6)2,所以所加试剂为铁氰化钾溶液K3[Fe(CN)6],
故答案为:K3[Fe(CN)6];
(6)综合上述实验分析,升高温度、提高FeCl3溶液的酸性会加快反应速率,缩短浅绿色出现的时间,
故答案为:加热或提高FeCl3溶液的酸性会缩短浅绿色出现的时间.
点评 本题为SO2的性质探究实验,涉及装置气密性的检验,尾气吸收,及物质的量浓度溶液的配制,题目难度中等.

| A. | $\frac{bc}{a{N}_{A}}$ | B. | $\frac{ac}{b{N}_{A}}$ | C. | $\frac{ab}{c{N}_{A}}$ | D. | $\frac{b}{ac{N}_{A}}$ |
| A. | 含H+的溶液一定呈酸性 | |
| B. | pH=7的溶液一定呈中性 | |
| C. | c(OH-)═c(H+)的溶液一定呈中性 | |
| D. | 水中加入硫酸恢复至室温后,Kw=c(H+)•c(OH-)将变大 |
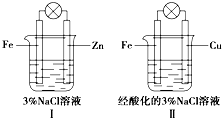
| A. | Ⅰ和Ⅱ中正极均被保护 | |
| B. | Ⅰ和Ⅱ中负极反应均是Fe-2e-═Fe2+ | |
| C. | Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-═4OH- | |
| D. | Ⅰ和Ⅱ中灯泡均会发亮 |
 电解原理在化学工业中有广泛应用.下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)X的电极名称是阴极.
(2)若X、Y都是惰性电极,a是硝酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,Y极上的电极反应式为2H2O-4e-=4H++O2↑,一段时间后,在X极附近观察到的现象是有气泡,溶液变红.
(3)若X、Y都是惰性电极,a是足量的AgNO3溶液,写出电解过程的化学方程式4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3 ,电解一段时间,当电极上通过的电子为0.2mol时,阴极上生成物的质量为21.5g.
(4)若要用电镀方法在铁表面镀一层金属铜,应该选择的方案是D.
| 方案 | X | Y | a溶液 |
| A | 铜 | 石墨 | CuSO4 |
| B | 铜 | 铁 | CuSO4 |
| C | 铁 | 铜 | Fe(NO3)3 |
| D | 铁 | 铜 | CuSO4 |

实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36qo盐酸15mL、水.
(1)反应①的化学方程式为NH4[CuCl2]=CuCl↓+NH4Cl,用95%乙醇代替蒸馏水洗涤的主要目的是避免CuCl溶于水而造成损耗,洗去晶体表面的杂质离子及水分.
(2)本实验中通入O2的速率不宜过大,为便于观察和控制产生02的速率,宜选择图3中的B(填字母序号)方案.
(3)实验开始时,温度计显示反应液温度低于室温,主要原因是氯化铵溶于水吸收大量热量;电炉加热升温至50℃时停止加热,反应快速进行,烧瓶上方气体颜色逐渐由无色变为红棕色;当烧瓶上方红棕色气体逐渐变为无色时停止通入氧气,打开瓶塞,沿a或c(填字母)口倾出棕色反应液于l000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出.
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题有防止CuCl被氧化,避光防止分解.
(5)氯化亚铜的定量分析:
①称取样品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;玻璃珠的作用是加速样品的溶解.
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0mol.L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表.
(已知:CuCl+FeCl3═CuCl2+FeCl2,Fe2++Ce4+═Fe3++Ce3+)
| 实验序号 | 1 | 2 | 3 |
| 滴定起始读数(mL) | 0.75 | 0.50 | 0.80 |
| 滴定终点读数(mL) | 24.65 | 24.75 | 24.70 |
| A. | 化合物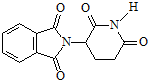 的分子式为C13H9O4N2 的分子式为C13H9O4N2 | |
| B. | 在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH | |
| C. | 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应 | |
| D. | 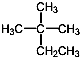 的系统命名为2-甲基-2-乙基丙烷 的系统命名为2-甲基-2-乙基丙烷 |
| A. | 2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | B. | I2+SO2+2H2O═H2SO4+2HI | ||
| C. | H2O2+H2SO4═SO2+O2↑+H2O | D. | 2Fe3++2I-═2Fe2++I2 |
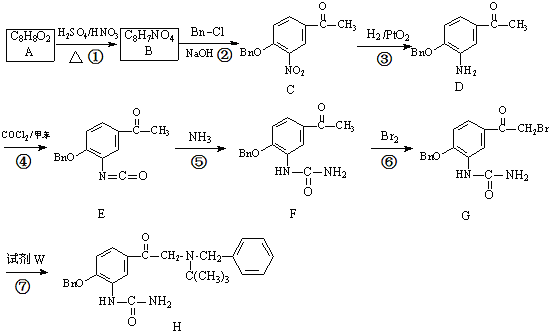
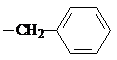 试剂W
试剂W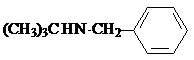 .
.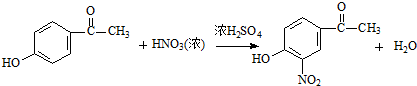 .
.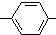 CH2
CH2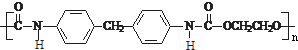 .
.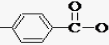 -CH2CH2N(C2H5)2(无机试剂任用)
-CH2CH2N(C2H5)2(无机试剂任用)