题目内容
如图,学生甲已将四种物质按照一定分类标准分类归入到椭圆形中,下列说法正确的是( )
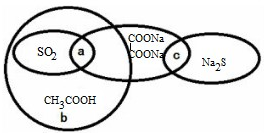

| A、SO2的水溶液能导电,所以SO2是电解质 |
| B、b可以代表含氧元素的离子化合物 |
| C、SO2、Na2C2O4均可作还原剂使酸性KMnO4溶液褪色 |
| D、CH3COOH与Na2S的反应称为酸碱中和反应 |
考点:电解质与非电解质,离子化合物的结构特征与性质,化学基本反应类型,二氧化硫的化学性质
专题:物质的分类专题
分析:A.二氧化硫的水溶液中导电离子不是二氧化硫电离的,二氧化硫为非电解质;
B.b表示含氧共价化合物,不是离子化合物;
C.二氧化硫和草酸钠都具有还原性,能够被酸性高锰酸钾溶液氧化;
D.醋酸酸性大于氢硫酸,醋酸能够与硫化钠反应生成草酸钠和硫化氢.
B.b表示含氧共价化合物,不是离子化合物;
C.二氧化硫和草酸钠都具有还原性,能够被酸性高锰酸钾溶液氧化;
D.醋酸酸性大于氢硫酸,醋酸能够与硫化钠反应生成草酸钠和硫化氢.
解答:
解:A.SO2的水溶液能导电,溶液中导电离子是亚硫酸电离的,亚硫酸为电解质,而二氧化硫为非电解质,故A错误;
B.根据图示可知,二氧化硫和醋酸都是共价化合物,所以b表示的是含氧的共价化合物,故B错误;
C.SO2、Na2C2O4均具有较强还原性,能够别强氧化性酸性高锰酸钾溶液氧化,同时使高锰酸钾溶液溶液褪色,故C正确;
D.醋酸属于酸,但是硫化钠为盐,该反应不属于酸碱中和反应反应,故D错误;
故选C.
B.根据图示可知,二氧化硫和醋酸都是共价化合物,所以b表示的是含氧的共价化合物,故B错误;
C.SO2、Na2C2O4均具有较强还原性,能够别强氧化性酸性高锰酸钾溶液氧化,同时使高锰酸钾溶液溶液褪色,故C正确;
D.醋酸属于酸,但是硫化钠为盐,该反应不属于酸碱中和反应反应,故D错误;
故选C.
点评:本题考查了电解质与非电解质、离子化合物与共价化合物、化学反应基本类型等知识,题目难度不大,注意掌握电解质与非电解质的概念,明确离子化合物与共价化合物的区别.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
下列反应属于氧化还原反应且焓变大于0的是( )
| A、Ba(OH)2?8H2O和NH4Cl反应 |
| B、Zn和稀H2SO4反应制氢气 |
| C、灼热的炭与水蒸气反应 |
| D、工业合成氨的反应 |
下列有关元素及其化合物性质的比较正确的是( )
| A、原子半径:F<O<Al |
| B、稳定性:H2O<PH3<NH3 |
| C、酸性:H2CO3<H2SO4<H3PO4 |
| D、碱性:LiOH<NaOH<Al(OH)3 |
 贝诺酯是一种治疗类风湿险关节炎药物,其结构简式如图所示,下列关于贝诺酷的描述正确的是( )
贝诺酯是一种治疗类风湿险关节炎药物,其结构简式如图所示,下列关于贝诺酷的描述正确的是( )| A、贝诺酷使溴水和酸性高锰酸钾溶液褪色的原理相同 |
| B、贝诺醋中含有3种含氧官能团 |
| C、1 mol贝诺酷最多可以消耗9 mol H2 |
| D、1 mol贝诺醋最多可以消耗5 mol NaOH |
下列各组物质中,常温下能起反应并产生氢气的是( )
| A、炭与浓硝酸 |
| B、铝与稀硫酸 |
| C、铁与浓硝酸 |
| D、铜与浓硫酸 |
下列说法不正确的是( )
| A、硫既可作氧化剂,也可作还原剂 |
| B、硫酸铜晶体中加入浓硫酸,蓝色晶体变为白色粉末,是因为浓硫酸具有脱水性 |
| C、可用铁罐贮运冷的浓硫酸 |
| D、医药上常用硫酸钡作X射线透视肠胃的内服药剂 |
下列关于胶体的叙述正确的是( )
| A、布朗运动是胶体粒子特有的运动方式,可以据此把胶体、溶液和悬浊液区分开来 |
| B、胶体和溶液的本质区别是胶体能发生丁达尔效应 |
| C、用过滤的方法可以分离胶体和悬浊液 |
| D、胶体带电,故在电场作用下会产生电泳现象 |
乙醚是一种常用的麻醉剂,但乙醚在空气中放置易发生自动氧化反应生成1-乙氧基氢过氧化物,用化学方程式表示为:CH3CH2OCH2CH3+O2→CH3CH2CH(CH3)OOH.下列关于该反应的说法正确的是( )
| A、O2中既有σ键又有π键 |
| B、该反应中,每消耗11.2L的氧气,乙醚失去的电子数为12.4×10-23 |
| C、1-乙氧基氢过氧化物中只有极性键没有非极性键 |
| D、起麻醉作用的是l-乙氧基氢过氧化物 |
下列叙述中正确的是( )
| A、由分子组成的物质中一定存在共价键 |
| B、由非金属组成的化合物不一定是共价化合物 |
| C、只有共价化合物里存在共价键 |
| D、离子化合物里只存在离子键 |