题目内容
乙醚是一种常用的麻醉剂,但乙醚在空气中放置易发生自动氧化反应生成1-乙氧基氢过氧化物,用化学方程式表示为:CH3CH2OCH2CH3+O2→CH3CH2CH(CH3)OOH.下列关于该反应的说法正确的是( )
| A、O2中既有σ键又有π键 |
| B、该反应中,每消耗11.2L的氧气,乙醚失去的电子数为12.4×10-23 |
| C、1-乙氧基氢过氧化物中只有极性键没有非极性键 |
| D、起麻醉作用的是l-乙氧基氢过氧化物 |
考点:氧化还原反应
专题:有机反应
分析:A.双键中含1个σ键、1个π键;
B.11.2L的氧气,不一定在标况下,不能计算其转移电子数;
C.1-乙氧基氢过氧化物中存在C-C、O-O键;
D.乙醚是一种常用的麻醉剂.
B.11.2L的氧气,不一定在标况下,不能计算其转移电子数;
C.1-乙氧基氢过氧化物中存在C-C、O-O键;
D.乙醚是一种常用的麻醉剂.
解答:
解:A.氧气的结构式为O=O,双键中含1个σ键、1个π键,则O2中既有σ键又有π键,故A正确;
B.11.2L的氧气,不一定在标况下,不能计算其转移电子数,若在标况下11.2L的氧气,乙醚失去的电子数为12.4×10-23,故B错误;
C.1-乙氧基氢过氧化物中存在C-C、O-O键非极性键和C-H极性键,1-乙氧基氢过氧化物中有极性键、非极性键,故C错误;
D.乙醚是一种常用的麻醉剂,起麻醉作用的是乙醚,故D错误;
故选A.
B.11.2L的氧气,不一定在标况下,不能计算其转移电子数,若在标况下11.2L的氧气,乙醚失去的电子数为12.4×10-23,故B错误;
C.1-乙氧基氢过氧化物中存在C-C、O-O键非极性键和C-H极性键,1-乙氧基氢过氧化物中有极性键、非极性键,故C错误;
D.乙醚是一种常用的麻醉剂,起麻醉作用的是乙醚,故D错误;
故选A.
点评:本题考查氧化还原反应与化学键,为高频考点,把握反应中氧气为氧化剂及判断化学键的一般规律为解答的关键,注意利用习题信息与所学知识的结合解决问题,题目难度不大,

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
下列说法正确的是( )
| A、简单甘油酯是纯净物,混合甘油酯是混合物 |
| B、植物油是一种良好的有机溶剂,可以用来萃取溴水中的溴单质 |
| C、天然油脂都是混合物,没有恒定的熔点、沸点 |
| D、纯天然高分子是纯净物,合成高聚物一定是混合物 |
如图,学生甲已将四种物质按照一定分类标准分类归入到椭圆形中,下列说法正确的是( )
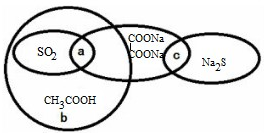

| A、SO2的水溶液能导电,所以SO2是电解质 |
| B、b可以代表含氧元素的离子化合物 |
| C、SO2、Na2C2O4均可作还原剂使酸性KMnO4溶液褪色 |
| D、CH3COOH与Na2S的反应称为酸碱中和反应 |
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属元素;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物对应的水化物为强碱 |
| D、XW2分子中各原子最外层电子未达到8电子结构 |
下列实验装置设计正确的是( )
A、 干燥氢气 |
B、 稀释浓硫酸 |
C、 可移动铜丝符合绿色化学要求 |
D、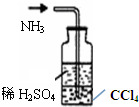 氨尾气吸收 |
对于固定体积的密闭容器中进行的气体反应A(g)+B(g)?C(g)+D(g),可以说明在恒温下该反应已达到平衡的是( )
| A、反应容器的压强不随时间而变化 |
| B、A气体和B气体的生成速率相等 |
| C、A气体和C气体的生成速率相等 |
| D、反应混合气体的密度不随时间而变化 |
在Cu与稀HNO3的反应中,若有1mol HNO3被还原,则被氧化的Cu的物质的量为( )
A、
| ||
B、
| ||
| C、3mol | ||
D、
|
下列数值表示有关元素的原子序数,各组数字中表示的元素的原子之间能形成离子键的是( )
| A、10 与 19 |
| B、6 与 16 |
| C、11 与 17 |
| D、14 与 8 |
 按要求问答下列问题
按要求问答下列问题