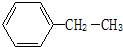
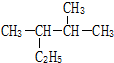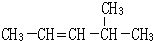题目内容
下列说法不正确的是( )
| A、硫既可作氧化剂,也可作还原剂 |
| B、硫酸铜晶体中加入浓硫酸,蓝色晶体变为白色粉末,是因为浓硫酸具有脱水性 |
| C、可用铁罐贮运冷的浓硫酸 |
| D、医药上常用硫酸钡作X射线透视肠胃的内服药剂 |
考点:浓硫酸的性质,含硫物质的性质及综合应用
专题:氧族元素
分析:A.硫元素化合价为0,处于中间价态;
B.浓硫酸吸收硫酸铜晶体中的水,使其变为白色的无水硫酸铜;
C.浓硫酸具有强氧化性,常温下使铁钝化;
D.硫酸钡为不溶于盐酸的沉淀.
B.浓硫酸吸收硫酸铜晶体中的水,使其变为白色的无水硫酸铜;
C.浓硫酸具有强氧化性,常温下使铁钝化;
D.硫酸钡为不溶于盐酸的沉淀.
解答:
解:A.硫元素化合价为0,处于中间价态,化合价可以升高和降低,所以既可作氧化剂,也可作还原剂,故A正确;
B.硫酸铜晶体中加入浓硫酸,蓝色晶体变为白色粉末,是因为浓硫酸具有吸水性,故B错误;
C.浓硫酸具有强氧化性,常温下使铁钝化,故C正确;
D.硫酸钡为不溶于盐酸的盐,医药上常用硫酸钡作X射线透视肠胃的内服药剂,故D正确;
故选:B.
B.硫酸铜晶体中加入浓硫酸,蓝色晶体变为白色粉末,是因为浓硫酸具有吸水性,故B错误;
C.浓硫酸具有强氧化性,常温下使铁钝化,故C正确;
D.硫酸钡为不溶于盐酸的盐,医药上常用硫酸钡作X射线透视肠胃的内服药剂,故D正确;
故选:B.
点评:本题侧重考查了浓硫酸的性质,题目难度不大,解题时注意浓硫酸吸水性和脱水性的区别.

练习册系列答案
相关题目
下列实验方案不合理的是( )
| A、加入饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸 |
| B、分离苯和硝基苯的混合物,可用蒸馏法 |
| C、可用苯将溴从溴苯中萃取出来 |
| D、可用水来鉴别苯、乙醇、四氯化碳 |
在一定温度下,容器内某一反应中M、N的物质的量n随反应时间t变化的曲线如图所示,下列表述中正确的是( )


| A、反应的化学方程式为2M?N |
| B、t2时V正=V逆,达到平衡 |
| C、t3时V正>V逆 |
| D、t1时浓度C(N)=2C(M) |
下列有关实验的说法错误的是( )
| A、除去苯中混有的苯酚,可加入浓溴水经充分振荡后过滤 |
| B、向1mL H2O2溶液中滴入几滴CuCl2饱和溶液,产生气泡的速率会加快 |
| C、向I2的CCl4溶液中加入浓的KI溶液后充分振荡,CCl4层的紫红色会变浅 |
| D、为获取与乙醛反应所需的Cu(OH)2,可向2mL 10% NaOH溶液中滴加大约5滴2% CuSO4溶液 |
如图,学生甲已将四种物质按照一定分类标准分类归入到椭圆形中,下列说法正确的是( )
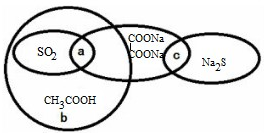

| A、SO2的水溶液能导电,所以SO2是电解质 |
| B、b可以代表含氧元素的离子化合物 |
| C、SO2、Na2C2O4均可作还原剂使酸性KMnO4溶液褪色 |
| D、CH3COOH与Na2S的反应称为酸碱中和反应 |
下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
A、 制溴苯 |
B、 实验室制取乙酸乙酯 |
C、 石油分馏 |
D、 实验室制取硝基苯 |
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属元素;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物对应的水化物为强碱 |
| D、XW2分子中各原子最外层电子未达到8电子结构 |
对于固定体积的密闭容器中进行的气体反应A(g)+B(g)?C(g)+D(g),可以说明在恒温下该反应已达到平衡的是( )
| A、反应容器的压强不随时间而变化 |
| B、A气体和B气体的生成速率相等 |
| C、A气体和C气体的生成速率相等 |
| D、反应混合气体的密度不随时间而变化 |