题目内容
下列叙述中正确的是( )
| A、由分子组成的物质中一定存在共价键 |
| B、由非金属组成的化合物不一定是共价化合物 |
| C、只有共价化合物里存在共价键 |
| D、离子化合物里只存在离子键 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:A.由分子组成的物质中不一定存在共价键;
B.由非金属元素组成的化合物不一定是共价化合物,可能是离子化合物;
C.离子化合物、多原子分子中可能含有共价键;
D.离子化合物中可能含有共价键.
B.由非金属元素组成的化合物不一定是共价化合物,可能是离子化合物;
C.离子化合物、多原子分子中可能含有共价键;
D.离子化合物中可能含有共价键.
解答:
解:A.由分子组成的物质中不一定存在共价键,稀有气体中不存在化学键,故A错误;
B.由非金属元素组成的化合物不一定是共价化合物,可能是离子化合物,如铵盐,故B正确;
C.离子化合物、多原子分子中可能含有共价键,如KOH、H2等,故C错误;
D.离子化合物中可能含有共价键,如NaOH,故D错误;
故选B.
B.由非金属元素组成的化合物不一定是共价化合物,可能是离子化合物,如铵盐,故B正确;
C.离子化合物、多原子分子中可能含有共价键,如KOH、H2等,故C错误;
D.离子化合物中可能含有共价键,如NaOH,故D错误;
故选B.
点评:本题考查了物质和化学键的关系,知道规律中的例外,易错选项是AC,稀有气体中只存在范德华力,不存在化学键,为易错点.

练习册系列答案
相关题目
如图,学生甲已将四种物质按照一定分类标准分类归入到椭圆形中,下列说法正确的是( )
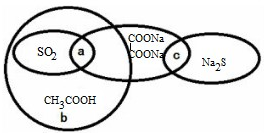

| A、SO2的水溶液能导电,所以SO2是电解质 |
| B、b可以代表含氧元素的离子化合物 |
| C、SO2、Na2C2O4均可作还原剂使酸性KMnO4溶液褪色 |
| D、CH3COOH与Na2S的反应称为酸碱中和反应 |
在Cu与稀HNO3的反应中,若有1mol HNO3被还原,则被氧化的Cu的物质的量为( )
A、
| ||
B、
| ||
| C、3mol | ||
D、
|
下列数值表示有关元素的原子序数,各组数字中表示的元素的原子之间能形成离子键的是( )
| A、10 与 19 |
| B、6 与 16 |
| C、11 与 17 |
| D、14 与 8 |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、室温下,42g乙烯和丙烯的混合气体中含有的碳原子数约为3NA |
| B、1mol C10H22分子中共价键总数为30NA |
| C、标准状况下,22.4 L四氯化碳的分子数为NA? |
| D、15g CH3+(碳正离子)中含有电子数为10NA |
几种短周期元素的原子半径及主要化合价见下表:
下列叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、L、R的单质与稀盐酸反应速率L<R |
| B、L与T形成的化合物具有两性 |
| C、Q、T两元素的氢化物热稳定性Q<T |
| D、L、Q形成的简单离子核外电子数相等 |
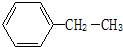
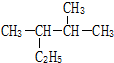
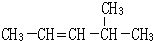
 按要求问答下列问题
按要求问答下列问题