题目内容
已知H-H,H-O,和O═O键的键能分别为436KJ.mol-1,463KJ.mol-1,495KJ.mol-1,下列热化学方程式正确的是( )
A、H2O(g)═H2(g)+1
| ||
B、H2O(g)═H2(g)+
| ||
| C、2 H2(g)+O2(g)═2 H2O(g)△H=+485 KJ.mol-1 | ||
| D、2 H2(g)+O2(g)═2 H2O(g)△H=-485 KJ.mol-1 |
考点:热化学方程式
专题:化学反应中的能量变化
分析:旧键断裂需要吸收能量,新键的生成会放出能量,△H=反应物的键能和-生成物的键能和,据此进行解答.
解答:
解:A.水分解是吸热反应,应该△H>0,故A错误;
B.H2O(g)═H2(g)+
O2(g),△H=反应物的键能和-生成物的键能和=2×463kJ/mol-436kJ/mol-
×495kJ/mol=+242.5kJ/mol,故B错误;
C.氢气燃烧放热,应该△H<0,故C错误;
D.2 H2(g)+O2(g)═2 H2O(g),△H=2×436kJ/mol+495kJ/mol-4×463kJ/mol=-485kJ/mol,故D正确;
故选:D.
B.H2O(g)═H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
C.氢气燃烧放热,应该△H<0,故C错误;
D.2 H2(g)+O2(g)═2 H2O(g),△H=2×436kJ/mol+495kJ/mol-4×463kJ/mol=-485kJ/mol,故D正确;
故选:D.
点评:本题考查了热化学方程式的书写、反应热的计算,题目难度不大,注意掌握热化学方程式的书写原则,明确化学键与化学反应中能量变化的关系是解题关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列解释事实的方程式不正确的是( )
| A、测0.1mol/L 氨水的pH为11:NH3?H2O?NH4++OH- | ||||
| B、将Na块放入水中,放出气体:2Na+2H2O═2NaOH+H2↑ | ||||
C、用CuCl2 溶液做导电实验,灯泡发光:CuCl2
| ||||
| D、Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2 ↑ |
对于某些离子的检验及结论中一定正确的是( )
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则一定有CO32- |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42- |
| C、分别含有Mg2+、Cu2+和Na+的三种盐酸盐溶液,用NaOH溶液就能一次鉴别开 |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |
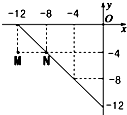 某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L.x与y的关系如图所示:
某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L.x与y的关系如图所示: