题目内容
17.下列过程一定涉及氧化还原反应的是( )| A. | 萃取 | B. | 电解 | C. | 净水 | D. | 分馏 |
分析 化学变化中存在元素的化合价变化,则为氧化还原反应,以此来解答.
解答 解:萃取、分馏均为物理变化,净化水可能利用吸附性或水解生成胶体等,则净水不一定发生化学变化,只有电解一定在阳极发生氧化反应,阴极发生还原反应,电解中存在元素的化合价变化,为氧化还原反应,
故选B.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.已知:常温下浓度为0.1mol/L的下列溶液的pH如表:下列有关说法不正确的是( )
| 溶质 | NaCl | Na2CO3 | NaClO | NaHCO3 |
| pH | 7 | 11.6 | 9.7 | 8.3 |
| A. | 在相同温度下,同浓度的三种酸溶液的导电能力:HCl>H2CO3>HClO | |
| B. | 等体积等物质的量浓度的NaCl溶液与NaClO溶液中Cl-和ClO-离子个数:Cl->ClO- | |
| C. | 向Na2CO3溶液中逐滴滴入少量稀盐酸,反应为:Na2CO3+2HCl=2NaCl+CO2↑+H2O | |
| D. | 若将CO2通入0.1mol/L Na2CO3溶液至溶液中性,则溶液中:2c(CO32-)+c(HCO3-)=0.2mol/L |
8.已知C3N4晶体具有比金刚石还大的硬度,且原子间均以单键结合.下列关于C3N4 晶体的说法正确的是( )
| A. | C3N4 晶体是分子晶体 | |
| B. | C3N4 晶体中微粒间通过离子键结合 | |
| C. | C3N4 晶体中C-N键的键长比金刚石中C-C键的键长要长 | |
| D. | C3N4 晶体中每个C原子连接4个N 原子,而每个N原子连接3个C原子 |
5.下列说法正确的是( )
| A. | 水晶、玛瑙、红宝石、蓝宝石的主要成分都是非金属氧化物 | |
| B. | 蛋白质是结构复杂的高分子化合物,蛋白质的生物活性首先取决于蛋白质的一级结构 | |
| C. | 同位素示踪法是研究化学反应历程的手段之一,红外光谱法可用于研究有机物分子结构,滴定法不能用于测量盐类物质溶液的浓度 | |
| D. | 丁达尔现象可用于区别溶液与胶体,云、雾、稀硫酸均能产生丁达尔现象 |
12.如表中实验“操作和现象”与“结论或目的一均正确的一组是( )
| 操作和现象 | 结论或目的 | |
| A | 向纯碱中滴加足量浓盐酸,将所得气体通入硅酸钠溶液中,溶液变浑浊 | 酸性:盐酸>碳酸>苯酚 |
| B | 取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO42- |
| C | 取少量Fe(NO3)2试样加水溶液后加稀硫酸酸化,滴加KSCN溶液,溶液变为红色 | 该Fe(NO3)2试样已经变质 |
| D | 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 | 目的:将不溶于酸的沉淀转化为易溶于酸的沉淀 |
| A. | A | B. | B | C. | C | D. | D |
2. 乙醇、乙酸都是有机化工重要的基础原料.
乙醇、乙酸都是有机化工重要的基础原料.
(1)空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(2)浓硫酸催化下,乙酸和乙醇生成乙酸乙酯
CH3COOH+CH3CH2OH$?_{110-120℃}^{H_{2}SO_{4}}$CH3COOH2CH3+H2O
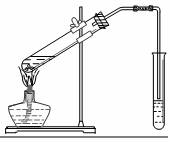
某化学兴趣小组的同学用如图装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是大试管中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙酸.
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止倒吸.
③相关物质的部分性质:
根据上表数据有同学提出可用水替代小试管中的Na2CO3溶液,你认为可行吗?说明理由:不能,乙酸乙酯在乙醇、乙酸和水的混合溶液中溶解度比较大.
④分离小试管中的乙酸乙酯应使用的仪器名称是分液漏斗;分离时,乙酸乙酯应该从仪器上口倒出(填“下口放”或“上口倒出”).
⑤兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如表:
表中数据X的范围是1.57-1.76mL;实验a与实验e探究的目的是探究乙酸用量对乙酸乙酯产量的影响.
 乙醇、乙酸都是有机化工重要的基础原料.
乙醇、乙酸都是有机化工重要的基础原料.(1)空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(2)浓硫酸催化下,乙酸和乙醇生成乙酸乙酯
CH3COOH+CH3CH2OH$?_{110-120℃}^{H_{2}SO_{4}}$CH3COOH2CH3+H2O
某化学兴趣小组的同学用如图装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是大试管中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙酸.
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止倒吸.
③相关物质的部分性质:
| 乙醇 | 乙酸 | 乙酸乙酯 | |
| 沸点 | 78.0℃ | 117.9℃ | 77.5℃ |
| 水溶性 | 易溶 | 易溶 | 难溶 |
④分离小试管中的乙酸乙酯应使用的仪器名称是分液漏斗;分离时,乙酸乙酯应该从仪器上口倒出(填“下口放”或“上口倒出”).
⑤兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如表:
| 实验序号 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| a | 2 | 2 | 1.33 |
| b | 3 | 2 | 1.57 |
| c | 4 | 2 | X |
| d | 5 | 2 | 1.76 |
| e | 2 | 3 | 1.55 |
9.设NA为阿伏伽德罗常数的数值.下列有关叙述正确的是( )
| A. | 12g由${\;}_{6}^{12}$C60和${\;}_{6}^{14}$C60组成的固体中的原子数为NA | |
| B. | 4.4g由CO2和N2O组成的混合气体中的电子数为2.2NA | |
| C. | 常温常压下22.4LNH3中所含的共价键数为3NA | |
| D. | 1L1mol•L-1次氯酸溶液中的ClO-数为NA |
6.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1L 1mol/L的盐酸中含HCl分子的数目为NA | |
| B. | 1 mol Cl2与足量的铁反应转移的电子数是3 NA | |
| C. | 常温常压下,15g乙烷分子中含有的共价键键数目为3.5NA | |
| D. | 标准状况下,4.48 L重水(D2O)中含有的中子数为2NA |
16.某无色溶液中,先加入足量稀盐酸,无任何变化,再加入BaCl2(aq),产生白色沉淀,则下列说法中正确的是( )
| A. | 无色溶液中一定含有SO42- | |
| B. | 无色溶液中一定含有Ag+ | |
| C. | 无色溶液中一定同时含有SO42-和Ag+ | |
| D. | 无色溶液中可能含有Ag+和SO42-中的一种或两种 |