题目内容
15.标准状况下,将NO2、NO、O2 混合并充满容器,然后把容器倒置于水槽中,充分反应后,水充满容器,则容器中HNO3溶液的物质的量的浓度(mol/L)用M表示范围是( )| A. | $\frac{1}{28}$<M<$\frac{1}{22.4}$ | B. | $\frac{1}{39.2}$<M<$\frac{1}{22.4}$ | C. | $\frac{1}{39.2}$<M<$\frac{1}{28}$ | D. | 0<M<$\frac{1}{22.4}$ |
分析 标准状况下,将NO2、NO、O2 混合并充满容器,然后把容器倒置于水槽中,充分反应后,容器中无气体剩余,利用端值法解答,可能发生:4NO2+O2+2H2O=4HNO3或4NO+3O2+2H2O=4HNO3,所得溶液为HNO3溶液,硝酸溶液体积等于混合气体的体积,结合方程式计算.
解答 解:标准状况下,将NO2、NO、O2 混合并充满容器,然后把容器倒置于水槽中,充分反应后,容器中无气体剩余,
若混合气体是NO2和O2,二者体积比一定为4:1,因为发生反应:4NO2+O2+2H2O=4HNO3,假设NO2为4mol,则生成硝酸为4mol,混合气体总物质的量为5mol,所得溶液的体积等于气体体积,所以所得溶液的物质的量浓度为:$\frac{4mol}{5mol×22.4L/mol}$mol/L=$\frac{1}{28}$mol/L;
若混合气体是NO和O2,二者体积比一定为4:3,因为发生反应:4NO+3O2+2H2O=4HNO3,假设NO2为4mol,则生成硝酸为4mol,混合气体总物质的量为7mol,所得溶液的体积等于气体体积,所以所得溶液的物质的量浓度为:$\frac{4mol}{7mol×22.4L/mol}$mol/L=$\frac{1}{39.2}$mol/L,
由于是NO、NO2、O2三种物质的混合物,则所得溶液浓度应介于$\frac{1}{39.2}$mol/L~$\frac{1}{28}$mol/L者之间,
故选C.
点评 本题考查有关NO2、NO和O2混合气体溶于水的计算,解决这类问题注意利用端值法结合反应的化学方程式计算,侧重考查学生分析解决问题的能力,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.在①丙烯 ②氟苯 ③四氯乙烯 ④甲苯四种有机化合物中,分子内所有原子均在同一平面的是( )
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
10.甲苯和甘油组成的混合物中,若碳元素的质量分数为0.63,那么可推知氢元素的质量分数为( )
| A. | 0.087 | B. | 0.174 | C. | 0.06 | D. | 无法确定 |
20.下列物质属于电解质的是( )
| A. | 熔融的氯化钠 | B. | CO2 | C. | 食盐水 | D. | Fe |
7.1mol乙烯与Cl2完全加成,其产物再与Cl2彻底取代,两个过程中共用Cl2( )
| A. | 2mol | B. | 4mol | C. | 5mol | D. | 6mol |
4.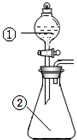 用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
 用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硫酸 | 用砂纸打磨过的铝条 | 无明显现象 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D | 稀硝酸 | 铜片 | 立即产生大量红棕色气体 |
| A. | A | B. | B | C. | C | D. | D |
5.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 78gNa2O2固体中含有阴离子的数目为2NA | |
| B. | 3.6g水含有极性键的数目为0.4NA | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA | |
| D. | 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |