题目内容
18. 将一张滤纸剪成四等份,用铜片、锌片、发光二极管、导线在玻璃片上连接成如图所示的装置,在四张滤纸上滴入稀H2SO4直至全部润湿.下列叙述正确的是( )
将一张滤纸剪成四等份,用铜片、锌片、发光二极管、导线在玻璃片上连接成如图所示的装置,在四张滤纸上滴入稀H2SO4直至全部润湿.下列叙述正确的是( )| A. | 锌片上有气泡,铜片溶解 | B. | 电子都是从铜片经外电路流向锌片 | ||
| C. | Zn片发生还原反应 | D. | 该装置至少有两种形式的能量转换 |
分析 该装置为四个原电池的串联电路,其中Zn为负极,被氧化,Cu为正极,原电池工作时,电子从负极经外电路流向正极,以此解答该题.
解答 解:A.锌为负极,铜为正极,正极上生成氢气,则铜片上有气泡,锌片溶解,故A错误;
B.电子从负极锌极经外电路流向正极铜极,故B错误;
C.锌为负极,发生氧化反应,故C错误;
D.该装置存在电能、化学能与电能与光能的转化,故D正确.
故选D.
点评 本题考查原电池的工作原理,为高频考点,题目难度不大,本题注意把握原电池正负极的判断以及电子、电流的流向.

练习册系列答案
相关题目
8.COCl2(g)?CO(g)+Cl2(g)△H>0,当反应达到平衡时,下列措施能提高COCl2转化率的是( )
①升温 ②恒容通入惰性气体 ③增加CO的浓度
④扩大容器体积 ⑤加催化剂 ⑥恒压通入惰性气体.
①升温 ②恒容通入惰性气体 ③增加CO的浓度
④扩大容器体积 ⑤加催化剂 ⑥恒压通入惰性气体.
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑥ | D. | ③⑤⑥ |
9.关于1mol/L K2SO4溶液的下列说法正确的是( )
| A. | 溶液中含有1mol K2SO4 | B. | 1molK2SO4溶于1L水中 | ||
| C. | 溶液中c(K+ )=2mol/L | D. | 1L 溶液中含2molK+,4mol O2- |
13.已烯雌酚是一种激素类药物,结构如图,下列有关叙述中不正确的是( )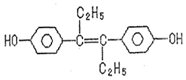

| A. | 可与NaOH和NaHCO3发生反应 | |
| B. | 可以用有机溶剂萃取 | |
| C. | 1mol该有机物可以与5molBr2发生反应 | |
| D. | 该有机物分子中,可能有18个碳原子共平面 |
3.“纳米材料”是粒子直径为1nm~100nm的材料,纳米碳就是其中的一种.某研究所将纳米碳均匀的分散到蒸馏水中,得到的物质:①是溶液 ②是胶体 ③具有丁达尔现象 ④不能透过半透膜 ⑤不能透过滤纸.其中正确的是( )
| A. | ①④⑥ | B. | ②③⑤ | C. | ②③④ | D. | ①③④⑥ |
10.有四种物质的量浓度相同且由一价阳离子A+、B+和一价阴离子X-、Y-组成的盐溶液,常温下AX溶液和BY溶液的pH都为7,AY溶液的pH<7,BX的溶液的pH>7.则可能不水解的盐是( )
| A. | AX | B. | BX | C. | AY | D. | BY |
2.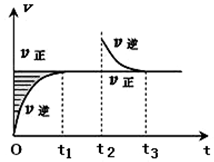 某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
 某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )| A. | Z和W在该条件下至少有一个是为气态 | |
| B. | t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 | |
| C. | 若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 | |
| D. | 若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等 |