题目内容
4.关于一个自发进行的放热反应,且属于氧化还原反应.下列叙述正确的是( )| A. | 反应不需要加热即可进行反应 | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 反应物的总键能高于生成物的总键能 | |
| D. | 理论上可以使该反应的化学能直接转化为电能 |
分析 A. 一个化学反应发生的条件与反应的热效应无关;
B.放热反应实质是反应物所具有的总能量高于生成物所具有的总能量;
C.放热反应是反应物的总键能低于生成物的总键能;
D.自发的氧化还原反应,可发生原电池反应.
解答 解:A.放热反应有的需加热,有的不需加热,如木炭的燃烧是一个放热反应,但需要点燃,点燃的目的是使其达到着火点,起动这个反应,再如铝热反应也是,故A错误;
B.放热反应实质是反应物所具有的总能量高于生成物所具有的总能量,故B错误;
C.反应物断键吸收能量,生成物成键放出能量,放热反应是吸得少,放得多,所以放热反应是反应物的总键能低于生成物的总键能,故C错误;
D.自发的氧化还原反应,可发生原电池反应,如Zn与稀硫酸的反应可发生原电池反应,原电池将化学能转化为电能,故D正确;
故选D.
点评 本题结合氧化还原反应、原电池考查了化学反应过程中的能量变化知识,注意把握反应的热效应与反应条件的关系,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列说法不正确的是( )
| A. | 利用盖斯定律可计算某些难以直接测量的反应焓变 | |
| B. | 如果一个热化学方程式可通过其他几个热化学方程式相加减而得到,则该反应的焓变可由相对应的热化学方程式的焓变相加减而得到 | |
| C. | 当同一个化学反应以不同的途径完成时,反应的焓变也是不同的 | |
| D. | 对于放热反应,放出的热量越多,焓变越小 |
15.下列对离子颜色说法不正确的是( )
| A. | Cu2+ 蓝色 | B. | MnO4-紫红色 | C. | Na+黄色 | D. | Fe3+棕黄色 |
12.类比推理是化学学习中的一种重要方法.下列类推结论正确的是( )
| 选项 | 类比对象 | 结论 |
| A | 2F2+2H2O═4HF+O2 | 2I2+H2O═4HI+O2↑ |
| B | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | 3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ |
| C | Na2O+H2O═2NaOH | FeO+H2O═Fe(OH)2 |
| D | Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O═CaSO3↓+2HClO |
| A. | A | B. | B | C. | C | D. | D |
16.各有机物的名称肯定错误的是( )
| A. | 2,2-二甲基丙烷 | B. | 3-甲基-2-丁烯 | C. | 4-甲基-1-戊炔 | D. | 1,3-二甲基苯 |
14.已知在25℃、1.0×105Pa条件下,2mol氢气燃烧生成水蒸气放出484KJ热量,下列热化学方程式正确的是( )
| A. | H2(g)+$\frac{1}{2}$ O2(g)═H2O(g)△H=+242 kJ/mol | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$ O2(g)═H2O(g)△H=-242kJ/mol | D. | 2H2(g)+O2(g)═2H2O(g)△H=+484 kJ/mol |
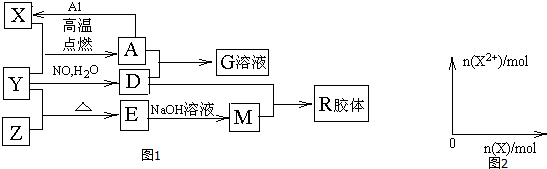
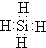 .
.